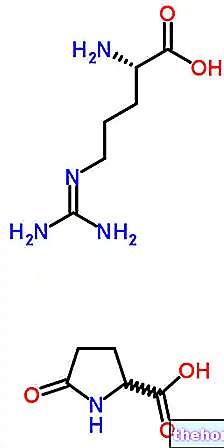
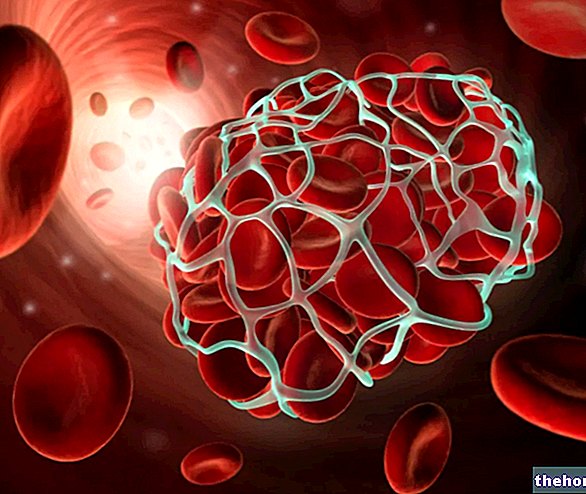
Struktura in funkcije
Hemoglobin je metaloprotein, ki ga vsebujejo rdeče krvne celice in je odgovoren za transport kisika v krvnem obtoku.Dejansko je kisik le zmerno topen v vodi; zato količine, raztopljene v krvi (manj kot 2% celotne količine), ne zadoščajo za zadovoljevanje presnovnih potreb tkiv. Potreba po posebnem prevozniku je torej očitna.
V krvnem obtoku se kisik ne more neposredno in reverzibilno vezati na beljakovine, kot se to zgodi namesto kovin, kot sta baker in železo. Ni presenetljivo, da v središču vsake proteinske podenote hemoglobina, zavite v beljakovinsko lupino, najdemo tako imenovano protetično skupina EME, s kovinskim srcem, ki ga predstavlja atom železa v oksidacijskem stanju Fe2 + (reducirano stanje), ki reverzibilno veže kisik.
Analiza krvi
- Normalne vrednosti hemoglobina v krvi: 13-17 g / 100 ml
Pri ženskah so te vrednosti v povprečju 5-10% nižje kot pri moških.
Možni vzroki visokega hemoglobina
- Policitemije
- Podaljšano bivanje na visokih tleh
- Kronične pljučne bolezni
- Srčna bolezen
- Krvni doping (uporaba eritropoetina in derivatov ali snovi, ki posnemajo njihovo delovanje)
Možni vzroki za nizek hemoglobin
- Anemije
- Pomanjkanje železa (pomanjkanje železa)
- Obilna krvavitev
- Karcinomi
- Nosečnost
- Thalassemias
- Opekline
Vsebnost kisika v krvi je torej podana z seštevanjem majhne količine, raztopljene v plazmi, z frakcijo, vezano na železo hemoglobin.
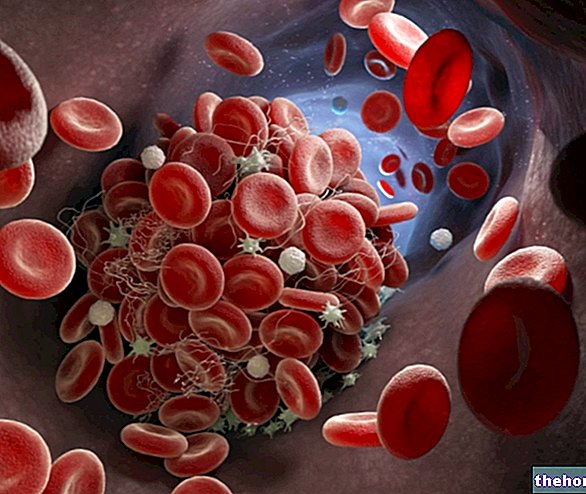
Več kot 98% kisika v krvi je vezanih na hemoglobin, ki nato kroži v krvnem obtoku, ki se nahaja znotraj rdečih krvnih celic, zato brez hemoglobina eritrociti ne bi mogli opravljati svoje naloge kot prenosniki kisika v krvi.
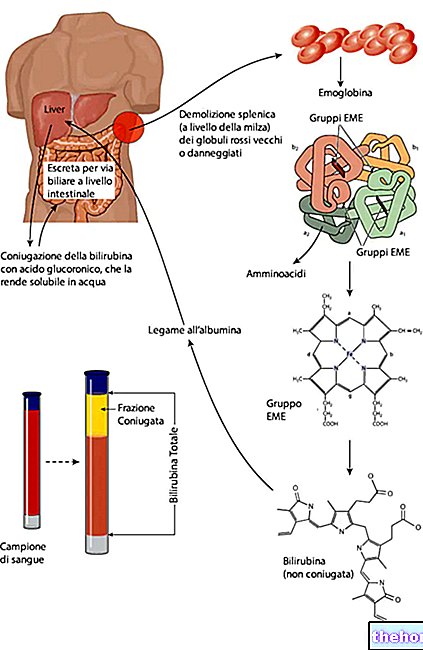
Glede na osrednjo vlogo te kovine sinteza hemoglobina zahteva ustrezen vnos železa v prehrano. Približno 70% železa v telesu je dejansko v hemovih skupinah hemoglobina.
Hemoglobin je sestavljen iz 4 podenot, ki so po strukturi zelo podobne mioglobinu *.
* Medtem ko hemoglobin prenaša kisik iz pljuč v tkiva, mioglobin prenaša kisik, ki ga sprošča hemoglobin, v različne celične organele, ki ga uporabljajo (npr. Mitohondrije).

Hemoglobin je velik in kompleksen metaloprotein, za katerega so značilne štiri kroglaste beljakovinske verige, ovite okoli skupine hema, ki vsebuje Fe2 +.
Za vsako molekulo hemoglobina zato najdemo štiri skupine hemov, zavitih v relativno kroglasto beljakovinsko verigo. Ker so v vsaki molekuli hemoglobina štirje atomi železa, lahko vsaka molekula hemoglobina veže štiri atome kisika nase, glede na reverzibilno reakcijo:
Hb + 4O2 ← → Hb (O2) 4
Kot je znano večini, je naloga hemoglobina, da vzame kisik v pljuča, ga sprosti v celice, ki ga potrebujejo, iz njih vzamejo ogljikov dioksid in ga sprostijo v pljuča, kjer se čilo znova začne.
Med prehodom krvi v kapilare pljučnih alveolov hemoglobin veže kisik nase, ki se nato sprosti v tkiva v perifernem obtoku. Do te izmenjave pride, ker so vezi kisika z železom skupine EME labilne in občutljive na številne dejavnike, med katerimi je najpomembnejši napetost ali parcialni tlak kisika.
Vezava kisika na hemoglobin in Bohrov učinek
V pljučih se napetost kisika v plazmi poveča zaradi difuzije plina iz alveolov v kri (↑ PO2); to povečanje povzroči, da se hemoglobin navdušeno veže na kisik; nasprotno se zgodi v perifernih tkivih, kjer se koncentracija raztopljenega kisika v krvi zmanjša (↓ PO2), parcialni tlak ogljikovega dioksida pa se poveča (↑ CO2); to povzroči, da hemoglobin sprosti kisik in se napolni s CO2. Čim bolj poenostavi koncept, več ogljikovega dioksida je v krvi, manj kisika ostane vezanega na hemoglobin.
Čeprav je količina kisika, ki se fizično raztopi v krvi, zelo majhna, ima ključno vlogo. Dejansko ta količina močno vpliva na trdnost vezi med kisikom in hemoglobinom (pa tudi predstavlja "pomembno referenčno vrednost pri uravnavanju pljučne ventilacije).
Če povzamemo vse z grafikonom, količina kisika, vezanega na hemoglobin, narašča glede na pO2 po sigmoidni krivulji:

Dejstvo, da je plato območje tako veliko, predstavlja pomembno mejo varnosti pri največji nasičenosti hemoglobina med prehodom v pljuča. tudi če je delni tlak kisika 70 mmHg (tipičen pojav nekaterih bolezni ali bivanje na velikih nadmorskih višinah), odstotki nasičenega hemoglobina ostanejo blizu 100%.
V območju največjega naklona, ko delna napetost kisika pade pod 40 mmHg, se sposobnost hemoglobina, da veže kisik, nenadoma zmanjša.
V mirovanju je PO2 v znotrajceličnih tekočinah približno 40 mmHg; na tem mestu se zaradi zakonov plinov kisik, raztopljen v plazmi, razprši proti revnejšim tkivom O2 in prečka kapilarno membrano, zato se plazemska napetost O2 še zniža, kar spodbuja sproščanje kisika iz hemoglobina. . Po drugi strani pa se med intenzivnim fizičnim naporom napetost kisika v tkivih spusti na 15 mmHg ali manj, zaradi česar se v krvi močno zmanjša kisik.
Kot rečeno, v mirovanju iz tkiv zapusti pomembna količina oksigeniranega hemoglobina, ki ostane na voljo v primeru potrebe (na primer za obvladovanje nenadnega povečanja presnove v nekaterih celicah).
Trdna črta, prikazana na zgornji sliki, se imenuje krivulja disociacije hemoglobina; običajno se določi in vitro pri pH 7,4 in pri temperaturi 37 ° C.
Bohrov učinek vpliva tako na vnos O2 na ravni pljuč kot na njegovo sproščanje na ravni tkiva.
Kjer je več raztopljenega ogljikovega dioksida v obliki bikarbonata, hemoglobin lažje sprošča kisik in se napolni z ogljikovim dioksidom (v obliki bikarbonata).

Enak učinek dosežemo z zakisljevanjem krvi: bolj ko se pH krvi zniža in manj kisika ostane vezanega na hemoglobin; ni presenetljivo, da se ogljikov dioksid v krvi raztopi predvsem v obliki ogljikove kisline, ki disociira.



V čast svojega odkritelja je učinek pH ali ogljikovega dioksida na disociacijo kisika znan kot Bohrov učinek.
Kot je bilo pričakovano, v kislem okolju hemoglobin lažje sprošča kisik, medtem ko je v osnovnem okolju vez s kisikom močnejša.

Drugi dejavniki, ki lahko spremenijo afiniteto hemoglobina do kisika, so temperatura. Zlasti se afiniteta hemoglobina do kisika zmanjšuje z naraščanjem telesne temperature. To je še posebej ugodno v zimskih in spomladanskih mesecih, saj temperatura pljučne krvi (v stiku s zrak zunanjega okolja) je nižji od tistega, ki ga dosežemo v tkivih, kjer se zato olajša sproščanje kisika.

2.3 difosfoglicerat je vmesni produkt pri glikolizi, ki vpliva na afiniteto hemoglobina do kisika. Če se njegove koncentracije v rdečih krvnih celicah povečajo, se afiniteta hemoglobina do kisika zmanjša, kar olajša sproščanje kisika v tkiva. Ni presenetljivo, da koncentracije eritrocitov 2,3 difosfoglicerata se poveča, na primer pri anemiji, srčno-pljučni insuficienci in med bivanjem na visoki nadmorski višini.
Na splošno je učinek 2,3 bisfosfoglicerata relativno počasen, zlasti v primerjavi s hitrim odzivom na spremembe pH, temperature in delnega tlaka ogljikovega dioksida.

Bohrov učinek je zelo pomemben pri intenzivnem mišičnem delu; v takšnih razmerah dejansko v tkivih, ki so najbolj izpostavljena stresu, pride do lokalnega zvišanja temperature in tlaka ogljikovega dioksida, torej kislosti krvi. Kot je razloženo zgoraj, vse to spodbuja sproščanje kisika v tkiva in premika krivuljo disociacije hemoglobina v desno.



.jpg)