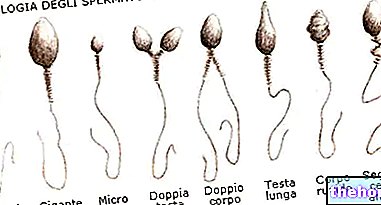
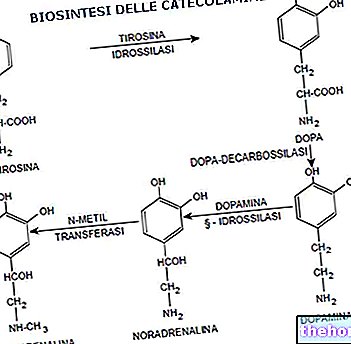
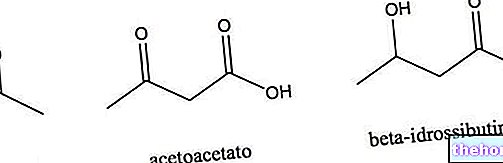
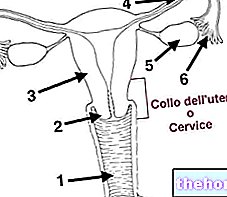
Aminokisline in beljakovine so vmesni produkti prehoda iz mineralnega sveta v živo snov.
Kot že ime pove, so aminokisline bifunkcionalne organske snovi: sestavljene iz amino funkcije (-NH2) in karboksilne funkcije (-COOH); lahko so α, β, γ itd., odvisno od položaja, ki ga zaseda amino skupina glede na karboksi skupino:



Biološko pomembne aminokisline so vse α-aminokisline.
Proteinske strukture sestavljajo dvajset aminokislin.
Kot je razvidno iz zgoraj prikazanih generičnih struktur, imajo vse aminokisline skupen del in drugačen del, ki jih označuje (na splošno predstavljen z R).
Od dvajsetih aminokislin je devetnajst optično aktivnih (odklonijo ravnino polarizirane svetlobe).
Večina aminokislin ima samo eno amino skupino in en karboksil, zato se imenujejo nevtralne aminokisline; imenujemo tiste, ki imajo dodaten karboksil kisle aminokisline medtem ko so tisti z dodatno amino skupino bazične aminokisline.
Aminokisline so kristalinične trdne snovi in imajo dobro topnost v vodi.
Pomanjkanje nekaterih aminokislin v prehrani povzroča resne spremembe v razvoju; pravzaprav človeški organizem ne more sintetizirati nekaterih aminokislin, ki se imenujejo esencialne (vnesti jih je treba s prehrano), medtem ko lahko sam proizvede le nekatere aminokisline (tiste, ki niso bistvene).
Ena od bolezni zaradi pomanjkanja esencialnih aminokislin je tista, ki je znana po imenu kwashiorkor (beseda, ki izvira iz afriškega narečja, kar v prevodu pomeni "prva in druga"); ta bolezen prizadene prvorojenca, vendar po rojstvu drugega otroka, ker prvemu otroku primanjkuje materinega mleka, ki vsebuje pravilno oskrbo z beljakovinami. Ta bolezen je zato razširjena med podhranjenimi prebivalci in vključuje drisko, pomanjkanje apetita, ki vodi v postopno oslabitev organizma.
Kot smo že omenili, imajo naravne aminokisline, razen glicina (to je a-aminokislina z vodikom namesto skupine R in je najmanjša od dvajsetih), ki imajo optično aktivnost zaradi prisotnosti vsaj ene asimetrične ogljika. V naravnih aminokislinah absolutna konfiguracija asimetričnega ogljika, na katerem sta vezani samo amino in karboksi skupine, pripada seriji L;
D-aminokisline nikoli ne postanejo del strukture beljakovin.
Spomnimo se, da:
DNA ---- transkripcija → m-RNA ---- prevod → beljakovina
Transkripcija se lahko kodira kot L-aminokisline; D-aminokisline so lahko v ne-beljakovinskih strukturah (npr. V sluznični steni bakterij: pri bakterijah ni "genetskih podatkov o tem, da imajo D-aminokisline za zaščitno vlogo, vendar obstajajo" genetske informacije za encime ki se ukvarjajo s steno obloge bakterij).
Vrnimo se k aminokislinam: drugačna struktura skupine R opredeljuje posamezne značilnosti vsake aminokisline in daje poseben prispevek k značilnostim beljakovin.
Zato je veljalo, da se aminokisline delijo glede na naravo skupine R:
Polarne, a nenapolnjene aminokisline:
Glicin (R = H-)
Serin (R = HO-CH2-)
Treoninbistvenega pomena
Treonin ima dva središča simetrije: v naravi obstaja le 2S, 3R treonin.
Treonin je esencialna aminokislina (ne smemo je zamenjati z nepogrešljivo: vse aminokisline so esencialne), zato jo je treba jemati s prehrano, torej z uživanjem hrane, ki jo vsebuje, ker, kot že omenjeno, genetska dediščina ni prisotna v celice človeka, ki lahko proizvajajo to aminokislino (ta dediščina je prisotna v številnih rastlinah in boljših).
Hidroksilno skupino serina in treonina lahko esterificiramo s fosforilno skupino (dobimo fosfoserin in fosfotreonin), ta postopek se imenuje fosforilacija; fosforilacija se v naravi uporablja za prevajanje signalov med notranjostjo in zunanjostjo celice.
Cistein (R = HS-CH2-)
Sulfhidril cisteina je lažje prenašati kot hidroksil serina: žveplo in kisik sta šesti skupini, vendar je žveplo lažje oksidirati, ker ima večje dimenzije.
Tirozin [R = HO- (C6H4) -CH2-]
N.B.
(C6H4) = di-substituiran benzenski obroč
Tako kot pri serinu in treoninu lahko tudi hidroksil esterificiramo (fosforiliramo).Asparagin (R = NH2-CO-CH2-)
Glutamin (R = NH2-CO-CH2-CH2-)
Nepolarne aminokisline
imajo hidrofobne stranske skupine; v tem razredu ločimo:
Alifatika:
Alanin (R = CH3-)
Valin (R = (CH3) 2-CH-) bistven
Levcin (R = (CH3) 2-CH-CH2-) bistven
Izolevcin (R =
) bistveno
Bistven je metionin (R = CH3-S-CH2-CH2-)
Celične membrane so sestavljene iz lipidnega dvosloja z beljakovinami, zasidranimi zaradi njihovega hidrofobnega značaja, zato vsebujejo alanin, valin, izolevcin in levcin. Metionin pa je aminokislina, ki je skoraj vedno prisotna v majhnih količinah (približno 1%).
Prolin
Aromatično:
Fenilalanin (R = Ph-CH2-) Ph = fenil: esencialni mono substituiran benzen
Triptofan (R =
bistvenega pomena
Ti dve aminokislini, ki sta aromatski, absorbirata blizu ultravijoličnega sevanja (približno 300 nm); zato je mogoče uporabiti tehniko UV spektrofotometrije za določanje koncentracije znanega proteina, ki vsebuje te aminokisline.
Napolnjene aminokisline
Po drugi strani so razdeljeni na:
Kisle aminokisline (ki imajo polarne ostanke z negativnim nabojem pri pH 7) so takšne, ker lahko dajo pozitiven naboj H +:
Asparaginska kislina
Glutaminska kislina (R =
)
Te aminokisline izvirajo iz asparagina in glutamina; vsi štirje obstajajo v naravi in to pomeni, da je c "posebna informacija za vsakega izmed njih, to je c" je osnovni trojček v DNK, ki kodira vsakega od njih.
Osnovne aminokisline (ki imajo polarne ostanke s pozitivnim nabojem pri pH 7) so takšne, ker lahko sprejmejo pozitiven naboj H +:
Lizin (R =
) bistveno
Arginin (R =
)
Histidin (R =
)
Obstajajo beljakovine, v katerih so derivati aminokislin v stranskih verigah: na primer je lahko prisoten fosfoserin (ni genetskih podatkov, ki bi kodirali fosfoserin, le tisti za serin); fosfoserin je sprememba postprevajalsko: po sintezi beljakovin
DNA ---- transkripcija → m-RNA ---- prevod → beljakovina
takšne posttranslacijske modifikacije se lahko pojavijo na stranskih verigah proteina.
Glej tudi: Beljakovine, pogled na kemijo