Zdravilne učinkovine: Omalizumab
Xolair 75 mg prašek in vehikel za raztopino za injiciranje
Paketni vložki Xolair so na voljo za velikosti pakiranj:- Xolair 75 mg prašek in vehikel za raztopino za injiciranje
- Xolair 150 mg prašek in vehikel za raztopino za injiciranje
Zakaj se uporablja zdravilo Xolair? Za kaj je to?
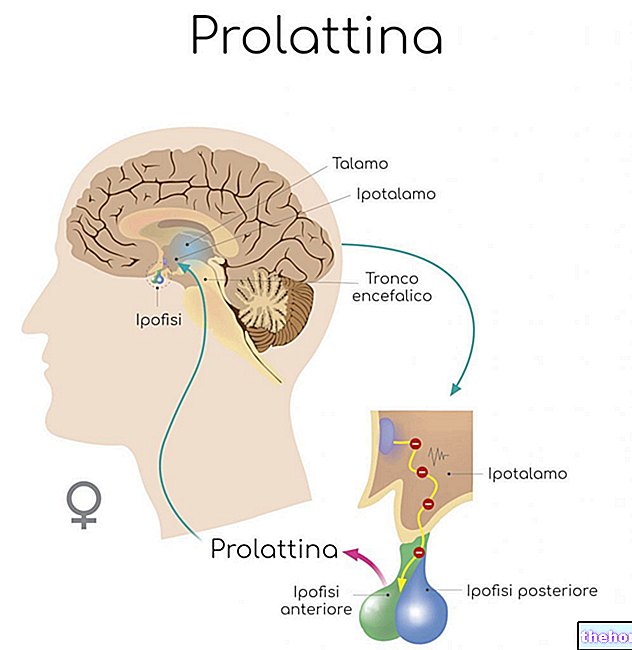
Zdravilna učinkovina zdravila Xolair je omalizumab. Omalizumab je sintetična beljakovina, podobna naravnim beljakovinam, ki jih proizvaja telo; spada v razred zdravil, imenovanih monoklonska protitelesa.
Uporablja se za preprečevanje poslabšanja astme z nadzorovanjem simptomov hude alergijske astme pri odraslih in mladostnikih (12 let in več) in otrocih (starih od 6 do manj kot 12 let), ki že prejemajo zdravila za astmo, vendar pri katerih simptomi astme niso dobro nadzorovani z zdravili, kot so visoki odmerki inhalacijskih steroidov ali inhalacijskih beta-agonistov.
Xolair blokira snov, imenovano imunoglobulin E (IgE), ki jo proizvaja telo.IgE ima ključno vlogo pri povzročanju alergijske astme.
Kontraindikacije Kadar zdravila Xolair ne smete uporabljati
Zdravila Xolair vam ne smejo dati
- če ste alergični na omalizumab ali katero koli sestavino tega zdravila (navedeno v poglavju 6).
Če menite, da ste alergični na katero koli sestavino, povejte svojemu zdravniku, ker vam zdravila Xolair ne smejo dati.
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Xolair
Xolair vsebuje beljakovine, pri nekaterih ljudeh pa lahko povzroči hude alergijske reakcije.
Znaki vključujejo izpuščaj, težave z dihanjem, oteklino ali občutek omedlevice. Če imate po jemanju zdravila Xolair alergijsko reakcijo, se čim prej obrnite na zdravnika.
Pri bolnikih, zdravljenih z zdravilom Xolair, so opazili posebno vrsto alergijske reakcije, imenovano serumska bolezen. Simptomi serumske bolezni so lahko eden ali več od naslednjih: bolečine v sklepih z oteklino ali otrplostjo ali brez nje, izpuščaj, zvišana telesna temperatura, otekle bezgavke, bolečine v mišicah. Če opazite katerega od teh simptomov ali zlasti kombinacijo teh simptomov, se nemudoma posvetujte z zdravnikom.
Pri bolnikih, zdravljenih z zdravilom Xolair, so opazili Churg-Straussov sindrom in eozinofilni sindrom. Simptomi so lahko eden ali več od naslednjih: otekanje, bolečina ali izpuščaj okoli krvnih ali limfnih žil, povišana raven določene vrste belih krvnih celic (izrazita eozinofilija), poslabšanje težav z dihanjem, zamašen nos, težave s srcem, bolečina, odrevenelost , mravljinčenje v rokah in nogah. Če opazite katerega od teh simptomov, zlasti če imate kombinacijo teh simptomov, se nemudoma posvetujte z zdravnikom.
Pred dajanjem zdravila Xolair se posvetujte s svojim zdravnikom:
- če imate težave z ledvicami ali jetri
- če imate motnjo, pri kateri vaš imunski sistem napade del telesa (avtoimunska bolezen)
- če živite v regijah, kjer so pogoste okužbe, ki jih povzročajo paraziti, ali če nameravate potovati v eno od teh regij, ker lahko zdravilo Xolair zmanjša vašo odpornost na te okužbe.
Zdravilo Xolair ne zdravi akutnih simptomov astme, kot je nenaden napad astme. Zato se zdravila Xolair ne sme uporabljati za zdravljenje teh simptomov.
Ne uporabljajte zdravila Xolair za preprečevanje ali zdravljenje drugih motenj alergijskega tipa, kot so nenadne alergijske reakcije, sindrom hiperimunoglobulina E (dedna imunska motnja), aspergiloza (glivična pljučna bolezen), alergija na hrano, ekcem ali seneni nahod, ker zdravila Xolair niso preučevali v teh pogojih.
Otroci (mlajši od 6 let)
Zdravila Xolair se ne sme dajati otrokom, mlajšim od 6 let. V tej starostni skupini ni dovolj podatkov.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Xolair
Povejte svojemu zdravniku, farmacevtu ali medicinski sestri, če jemljete, ste pred kratkim jemali ali pa boste morda začeli jemati katero koli drugo zdravilo.
To je še posebej pomembno, če jemljete:
- zdravila za zdravljenje okužbe, ki jo povzroča parazit, saj lahko zdravilo Xolair zmanjša učinek teh zdravil,
- inhalacijske kortikosteroide in druga zdravila za alergijsko astmo.
Opozorila Pomembno je vedeti, da:
Nosečnost in dojenje
Med nosečnostjo vam zdravila Xolair ne smete dajati, razen če zdravnik meni, da je to potrebno.
Če nameravate zanositi, povejte svojemu zdravniku, preden začnete zdravljenje z zdravilom Xolair. Zdravnik se bo z vami pogovoril o koristih in možnih tveganjih jemanja tega zdravila med nosečnostjo.
Če med jemanjem zdravila Xolair zanosite, o tem nemudoma obvestite svojega zdravnika.
Če dojite, vam zdravila Xolair ne smete dati.
Vpliv na sposobnost upravljanja vozil in strojev
Ni verjetno, da bi zdravilo Xolair vplivalo na sposobnost vožnje in upravljanja s stroji.
Odmerjanje in način uporabe Kako uporabljati zdravilo Xolair: Odmerjanje
Navodila za uporabo zdravila Xolair so v razdelku "Informacije za zdravstvene delavce".
Zdravnik bo določil, koliko zdravila Xolair potrebujete in kako pogosto ga boste prejeli. To je odvisno od vaše telesne mase in rezultatov krvnega testa, opravljenega pred začetkom zdravljenja za merjenje ravni IgE v krvi.
Zdravnik ali medicinska sestra vam bosta zdravilo Xolair dala kot injekcijo pod kožo.
Previdno upoštevajte navodila zdravnika ali medicinske sestre.
Dani znesek
Dobili boste 1 do 4 injekcije hkrati, vsaka dva tedna ali vsake štiri tedne.
Med zdravljenjem z zdravilom Xolair še naprej jemljite trenutno zdravilo za astmo. Ne prenehajte jemati zdravil za astmo, ne da bi se prej posvetovali z zdravnikom.
Morda ne boste opazili takojšnjega izboljšanja astme po začetku zdravljenja z zdravilom Xolair. Popolni učinek običajno dosežemo po 12-16 tednih.
Uporaba pri otrocih in mladostnikih
Zdravilo Xolair se lahko uporablja pri otrocih in mladostnikih, starih 6 let ali več, ki že jemljejo zdravila za astmo, vendar simptomov astme ne uravnavajo dobro zdravila, kot so visoki odmerki inhalacijskih steroidov ali inhalacijski agonisti beta. Zdravnik bo vedel, koliko zdravila Xolair ima vaš otrok potrebe in kako pogosto jih bodo morali jemati. To bo odvisno od otrokove teže in rezultatov krvnega testa, opravljenega pred začetkom zdravljenja za merjenje količine IgE v otrokovi krvi.
Če niste vzeli odmerka zdravila Xolair
Čim prej se obrnite na svojega zdravnika ali bolnišnico, da se dogovorite za nov sestanek.
Če ste prenehali jemati zdravilo Xolair
Ne prenehajte jemati zdravila Xolair, razen če vam tako naroči zdravnik. Prekinitev ali prekinitev zdravljenja z zdravilom Xolair lahko povzroči ponovitev simptomov astme.
Če imate dodatna vprašanja o uporabi tega zdravila, se posvetujte z zdravnikom, farmacevtom ali medicinsko sestro.
Neželeni učinki Kakšni so neželeni učinki zdravila Xolair
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih. Neželeni učinki, ki jih povzroča zdravilo Xolair, so običajno blagi do zmerni, včasih pa so lahko resni.
Resni neželeni učinki vključujejo:
Redki neželeni učinki (pojavijo se lahko pri največ 1 od 1.000 bolnikov)
- Nenadne hude alergijske reakcije: če opazite nenadne hude znake alergije ali kombiniran pojav znakov, kot so izpuščaj, srbenje ali koprivnica na koži, otekanje obraza, ustnic, jezika, grla (glasilke), sapnika ali drugih delov telo, hiter srčni utrip, omotica in omotica, težko dihanje, piskanje ali težave z dihanjem ali kateri koli drugi novi simptom, o tem nemudoma obvestite svojega zdravnika ali medicinsko sestro. imate lahko po uporabi zdravila Xolair povečano tveganje za razvoj hude alergijske reakcije.
- Sistemski eritematozni lupus (SLE). Simptomi lahko vključujejo bolečine v mišicah, bolečine v sklepih in otekanje ter izpuščaj. Lahko se pokažejo tudi drugi simptomi, kot so zvišana telesna temperatura, izguba teže in utrujenost.
Neznana (pogostnosti iz razpoložljivih podatkov ni mogoče oceniti)
- Pojav enega ali več naslednjih simptomov: oteklina, bolečina ali izpuščaj okoli krvnih ali limfnih žil, povišana raven določene vrste belih krvnih celic (izrazita eozinofilija), poslabšanje težav z dihanjem, zamašen nos, težave s srcem, bolečina, odrevenelost , mravljinčenje v rokah, nogah (znaki tako imenovanega "Churg-Straussovega sindroma ali hipereozinofilnega sindroma").
- Nizko število trombocitov v krvi s simptomi, kot so krvavitev ali modrice, je lažje kot običajno.
- Pojav katerega koli od naslednjih simptomov, zlasti če je povezan: bolečine v sklepih z oteklino ali otrplostjo ali brez nje, izpuščaj, zvišana telesna temperatura, otekle bezgavke, bolečine v mišicah (znaki serumske bolezni).
Če opazite katerega od teh simptomov, takoj obvestite svojega zdravnika ali medicinsko sestro.
Drugi neželeni učinki vključujejo:
Zelo pogosti neželeni učinki (pojavijo se lahko pri več kot 1 od 10 bolnikov)
- zvišana telesna temperatura (pri otrocih)
Pogosti neželeni učinki (pojavijo se lahko pri največ 1 od 10 bolnikov)
- reakcije na mestu injiciranja, kot so bolečina, oteklina, srbenje in pordelost
- bolečine v zgornjem delu trebuha (pri otrocih)
- glavobol (zelo pogost pri otrocih)
Občasni neželeni učinki (pojavijo se lahko pri največ 1 od 100 bolnikov)
- občutek omotičnosti, zaspanosti ali utrujenosti
- mravljinčenje ali odrevenelost v rokah ali nogah
- omedlevica, nizek krvni tlak pri sedečem ali stoječem položaju (posturalna hipotenzija), zardevanje
- vneto grlo, kašelj, akutne težave z dihanjem
- slabost (slabost), driska, prebavne motnje
- srbenje, koprivnica, izpuščaj, povečana občutljivost kože na sonce
- povečanje telesne mase
- gripi podobni simptomi
- otekle roke
Redki neželeni učinki (pojavijo se lahko pri največ 1 od 1.000 bolnikov)
- okužba s paraziti
Neznana (pogostnosti iz razpoložljivih podatkov ni mogoče oceniti)
- bolečine v sklepih, otekanje mišic in sklepov
- izguba las
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom, farmacevtom ali medicinsko sestro.To vključuje vse možne neželene učinke, ki niso navedeni v tem navodilu. zagotovite več informacij o varnosti tega zdravila.
Potek in zadržanje
- Zdravilo shranjujte nedosegljivo otrokom!
- Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na nalepki.
- Shranjujte v hladilniku (2 ° C - 8 ° C). Ne zamrzujte.
Rok "> Druge informacije
Kaj vsebuje zdravilo Xolair
- Zdravilna učinkovina je omalizumab. Ena viala vsebuje 75 mg omalizumaba. Po rekonstituciji ena viala vsebuje 125 mg / ml omalizumaba (75 mg v 0,6 ml).
- Pomožne snovi so saharoza, L-histidin, L-histidinijev klorid monohidrat, polisorbat 20.
Izgled zdravila Xolair in vsebina pakiranja
Xolair 75 mg prašek in vehikel za raztopino za injiciranje sta na voljo v obliki belega do belkastega praška v majhni stekleni viali skupaj z vialo, ki vsebuje 2 ml vode za injekcije. Preden si ga injicira zdravnik ali medicinska sestra, se prašek rekonstituira v vodi.
Xolair je na voljo v pakiranjih, ki vsebujejo eno vialo praška za raztopino za injiciranje in eno ampulo z 2 ml vode za injekcije.
Zdravilo Xolair je na voljo tudi v vialah, ki vsebujejo 150 mg omalizumaba.
Rok "> Informacije za zdravstvene delavce
Naslednje informacije so namenjene samo zdravstvenim delavcem:
Liofilizirano zdravilo se raztopi 15-20 minut, čeprav lahko v nekaterih primerih traja dlje. Popolnoma pripravljeno zdravilo je bistro do rahlo opalescentno, brezbarvno do bledo rjavkasto rumeno in ima lahko majhne mehurčke ali peno okoli roba viale. Zaradi viskoznosti rekonstituiranega zdravila je treba pazljivo odstraniti vsa zdravila iz viale, preden iz brizge iztisnemo odvečni zrak ali raztopino, da dobimo 0,6 ml.
Če želite pripraviti viale zdravila Xolair 75 mg za subkutano dajanje, sledite tem navodilom:
- Iz viale potegnite 0,9 ml vode za injekcije v brizgo, opremljeno z veliko iglo velikosti 18.
- Vialo držite pokonci na ravni površini, vstavite iglo in vodo za injekcije prenesite v vialo, ki vsebuje liofiliziran prašek, po standardnih sterilnih tehnikah, tako da vodo za injekcije usmerite neposredno na prašek.
- Vialo držite pokonci, močno obrnite (ne tresite) približno 1 minuto, da se prašek enakomerno navlaži.
- Za lažje raztapljanje po zaključku 3. koraka nežno obrnite vialo za 5-10 sekund, približno vsakih 5 minut, da se raztopijo preostali trdni delci. Upoštevati je treba, da lahko v nekaterih primerih traja več kot 20 minut, da se prašek raztopi v tem primeru ponovite 4. korak, dokler v raztopini ni vidnih več gelastih delcev. Ko se zdravilo popolnoma raztopi, v raztopini ne sme biti vidnih gelom podobnih delcev. Majhni mehurčki ali pena okoli roba viale so pogosti Pripravljeno zdravilo bo videti bistro do rahlo opalescentno, brezbarvno do bledo rjavkasto rumeno. Ne uporabljajte, če so prisotni trdni delci.
- Vialo obrnite vsaj 15 sekund, da raztopina steče v zamašek. Z novo 3 -mililitrsko brizgo, opremljeno z veliko iglo velikosti 18, vstavite iglo v vialo, obrnjeno navzdol.Če vialo držite obrnjeno navzdol, položite konico igle na dno raztopine v viali, ko raztopino vlečete v brizgo. Preden iglo odstranite iz viale, bat povlecite do konca soda brizge, da povlečete vso raztopino iz obrnjene viale.
- Za subkutano injiciranje zamenjajte iglo 18 z iglo s premerom 25.
- Izločite zrak, večje mehurčke in morebitno odvečno raztopino, da dobite zahtevano 0,6 ml raztopine. Na vrhu raztopine v brizgi lahko ostane tanka plast majhnih mehurčkov. Ker je raztopina rahlo viskozna, lahko dajanje raztopine z injekcijo pod kožo traja 5-10 sekund. Viala daje 0,6 ml (75 mg) zdravila Xolair.
- Injekcije se injicirajo subkutano v deltoidno področje roke ali v stegno.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA -
XOLAIR 75 mg prah in topilo za injiciranje raztapljanja
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA -
Ena viala vsebuje 75 mg omalizumaba *.
Po rekonstituciji ena viala vsebuje 125 mg / ml omalizumaba (75 mg v 0,6 ml).
* Omalizumab je humanizirano monoklonsko protitelo, proizvedeno s tehnologijo rekombinantne DNA v celični liniji jajčnika kitajskega hrčka (CHO).
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA -
Prašek in vehikel za raztopino za injiciranje.
Sivobel liofiliziran prašek.
04.0 KLINIČNE INFORMACIJE -
04.1 Terapevtske indikacije -
Zdravilo Xolair je indicirano pri odraslih, mladostnikih in otrocih, starih od 6 do
Zdravljenje z zdravilom Xolair je treba upoštevati le pri bolnikih z znano astmo, posredovano z IgE (imunoglobulin E) (glejte poglavje 4.2).
Odrasli in mladostniki (stari 12 let ali več)
Zdravilo Xolair je indicirano kot dodatno zdravljenje za izboljšanje nadzora astme pri bolnikih s hudo dolgotrajno alergijsko astmo kot pri preskusu kože ali reaktivnosti. in vitro pozitivni na večletni aeroalergen in zmanjšano delovanje pljuč (dnevni simptomi FEV1 ali nočno prebujanje in pri bolnikih z dokumentiranimi hudimi ponavljajočimi se poslabšanji astme, kljub vsakodnevnemu vnosu visokih odmerkov inhalacijskih kortikosteroidov in dolgotrajnem trajanju agonista beta2 z vdihavanjem.
Otroci (od 6
Zdravilo Xolair je indicirano kot dodatno zdravljenje za izboljšanje nadzora astme pri bolnikih s hudo dolgotrajno alergijsko astmo kot pri preskusu kože ali reaktivnosti. in vitro pozitiven na večletni aeroalergen in imajo pogoste dnevne simptome ali nočna prebujanja ter pri bolnikih z dokumentiranimi ponavljajočimi se hudimi poslabšanji astme, kljub vsakodnevnemu vnosu visokih odmerkov inhalacijskih kortikosteroidov in dolgo delujočega agonista beta2 z inhalacijo.
04.2 Odmerjanje in način uporabe -
Zdravljenje z zdravilom Xolair morajo začeti zdravniki z izkušnjami pri diagnosticiranju in zdravljenju hude vztrajne astme.
Odmerjanje
Ustrezni odmerek in pogostost dajanja zdravila Xolair sta odvisna od izhodiščnih ravni IgE (ie / ml), izmerjenih pred začetkom zdravljenja, in telesne mase (kg). Pred dajanjem začetnega odmerka morajo bolniki za določitev svojega odmerka določiti raven IgE s katerim koli komercialno dostopnim serumskim testom skupnega IgE. Na podlagi teh določitev bo morda za vsako dajanje potrebnih 75 do 600 mg zdravila Xolair v 1-4 injekcijah.
Manj verjetno je, da bodo koristi opažene pri bolnikih z ravnjo IgE pod 76 ie / ml (glejte poglavje 5.1). Pred začetkom zdravljenja mora zdravnik zagotoviti, da bodo odrasli in mladostniki s koncentracijo IgE pod 76 ie / ml in otroci (od 6 do in vitro (RAST)) na trajni alergen.
Glejte preglednico 1 za pretvorbo in preglednici 2 in 3 za določanje odmerka pri odraslih, mladostnikih in otrocih od 6 do
Bolnikom, pri katerih izhodiščne ravni IgE ali telesna teža v kilogramih presegajo meje tabele odmerkov, se zdravila Xolair ne sme dajati.
Največji priporočeni odmerek je 600 mg omalizumaba vsaka dva tedna.
Preglednica 1: Pretvorba iz odmerka v število vial, število injekcij in skupni volumen, vbrizgan pri vsaki uporabi
a0,6 ml = največji volumen, ki ga je mogoče izvleči na vialo (Xolair 75 mg).
b1,2 ml = največji volumen, ki ga je mogoče izvleči na vialo (Xolair 150 mg).
ali uporabite 0,6 ml iz 150 mg viale.
Tabela 2: UPRAVA VSAKE 4 TEDNE. Odmerki zdravila Xolair (miligrami na odmerek), ki se dajejo s subkutano injekcijo vsake 4 tedne
Tabela 3: UPRAVA VSAK 2 TEDNA. Odmerki zdravila Xolair (miligrami na odmerek), ki se dajejo s podkožno injekcijo vsaka 2 tedna
Trajanje zdravljenja, spremljanje in prilagajanje odmerka
Zdravilo Xolair je namenjeno dolgotrajnemu zdravljenju. Klinične študije so pokazale, da traja vsaj 12-16 tednov, da je zdravljenje z zdravilom Xolair učinkovito. Po 16 tednih od začetka zdravljenja z zdravilom Xolair mora zdravnik pregledati bolnike, da preveri, ali je zdravljenje učinkovito, preden se dajo nadaljnje injekcije. Odločitev o nadaljevanju zdravljenja z zdravilom Xolair ob koncu 16. tedna ali ob naslednjih priložnostih mora temeljiti na opazovanju izrazitega izboljšanja splošnega nadzora astme (glejte poglavje 5.1. Celotna ocena učinkovitosti zdravljenja pri zdravniku).
Prekinitev zdravljenja z zdravilom Xolair običajno povzroči vrnitev na povišane ravni prostega IgE in s tem povezane simptome. Skupne ravni IgE so med zdravljenjem povišane in ostanejo povišane še eno leto po prekinitvi zdravljenja. Zato ponovnega merjenja ravni IgE med zdravljenjem z zdravilom Xolair ni mogoče uporabiti kot vodilo za določitev odmerka. Določitev odmerka po "prekinitvi zdravljenja, ki traja manj kot eno leto, mora temeljiti na serumskih ravneh IgE, pridobljenih v času določanja začetnega odmerka. Če je bilo zdravljenje z zdravilom Xolair prekinjeno, je mogoče za določitev odmerka ponovno izmeriti celotne serumske ravni IgE. za leto ali več.
Odmerke je treba prilagoditi glede na pomembne spremembe telesne mase (glejte preglednici 2 in 3).
Posebne populacije
Starejši (65 let in več)
Podatkov o uporabi zdravila Xolair pri bolnikih, starejših od 65 let, je malo, vendar ni dokazov, da starejši bolniki potrebujejo drugačen odmerek kot mlajši odrasli bolniki.
Motnje delovanja ledvic ali jeter
Študije o vplivu okvare ledvic ali jeter na farmakokinetiko zdravila Xolair niso bile izvedene. čiščenje pri omalizumabu prevladuje retikulo-endotelijski sistem (RES), zato okvara ledvic ali jeter verjetno ne bo prizadeta. Čeprav posebnih odmerkov ni priporočljivo prilagajati, je treba pri teh bolnikih zdravilo Xolair dajati previdno (glejte poglavje 4.4).
Pediatrična populacija
Varnost in učinkovitost zdravila Xolair pri otrocih, mlajših od 6 let, nista bili ugotovljeni.
Način dajanja
Samo za subkutano dajanje. Ne dajajte intravensko ali intramuskularno.
Injekcije se dajejo subkutano v deltoidno področje roke. Druga možnost je, da se injekcije dajo v stegno, če obstajajo razlogi, ki onemogočajo dajanje v deltoidno regijo.
Izkušenj s samozdravljenjem z zdravilom Xolair je malo, zato naj zdravljenje izvaja le zdravstveni delavec.
Za navodila o rekonstituciji zdravila pred uporabo glejte poglavje 6.6 in razdelek z informacijami za zdravstvene delavce v navodilu za uporabo.
04.3 Kontraindikacije -
Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov, navedeno v poglavju 6.1.
04.4 Posebna opozorila in ustrezni previdnostni ukrepi pri uporabi -
Splošno
Zdravilo Xolair ni indicirano za zdravljenje akutnih poslabšanj astme, akutnega bronhospazma ali astme.
Zdravila Xolair niso preučevali pri bolnikih s sindromom hiperimunoglobulina E ali alergijsko bronhopulmonalno aspergilozo ali za preprečevanje anafilaktičnih reakcij, vključno z alergijami na hrano, atopijskim dermatitisom ali alergijskim rinitisom. Zdravilo Xolair ni indicirano za zdravljenje teh stanj.
Zdravljenja z zdravilom Xolair niso preučevali pri bolnikih z avtoimunskimi boleznimi, imunsko kompleksnimi stanji ali že obstoječo ledvično ali jetrno insuficienco (glejte poglavje 4.2). Pri dajanju zdravila Xolair tem skupinam bolnikov je potrebna previdnost.
Po začetku zdravljenja z zdravilom Xolair ni priporočljivo nenadoma prekiniti zdravljenja s sistemskimi ali inhalacijskimi kortikosteroidi. Zmanjšanje odmerkov kortikosteroidov je treba izvajati pod neposrednim zdravniškim nadzorom in ga je treba izvajati postopoma.
Motnje imunskega sistema
Alergijske reakcije tipa I
Pri omalizumabu se lahko pojavijo lokalne ali sistemske alergijske reakcije tipa I, vključno z anafilaksijo in anafilaktičnim šokom, tudi če se pojavijo po daljšem obdobju zdravljenja. Večina teh reakcij se pojavi v 2 urah po prvi in naslednji injekciji zdravila Xolair, nekatere pa so se pojavile tudi po 2 uri in celo več kot 24 ur po injiciranju. Zato morajo biti zdravila za zdravljenje anafilaktičnih reakcij vedno na voljo za takojšnjo uporabo po dajanju zdravila Xolair.
V kliničnih študijah so bile anafilaktične reakcije redke (glejte poglavje 4.8).
V kliničnih študijah so pri majhnem številu bolnikov odkrili protitelesa proti omalizumabu (glejte poglavje 4.8). Klinični pomen protiteles proti Xolairju ni dobro znan.
Serumska bolezen
Pri bolnikih, zdravljenih s humaniziranimi monoklonskimi protitelesi, vključno z omalizumabom, so opazili serumsko bolezen in reakcije, podobne serumski bolezni, ki so zapoznele alergijske reakcije tipa III. Predlagani patofiziološki mehanizem vključuje nastanek in odlaganje imunskih kompleksov po nastanku protiteles proti omalizumabu. ponavadi se pojavi 1-5 dni po prvi ali naslednji injekciji, tudi po daljšem trajanju zdravljenja. Simptomi, ki kažejo na serumsko bolezen, so artritis / artralgija, izpuščaj (urtikarija ali druge oblike), zvišana telesna temperatura in limfadenopatija. pri preprečevanju ali zdravljenju teh motenj in bolnikom je treba svetovati, naj poročajo o vseh sumljivih simptomih.
Churg-Straussov sindrom in hipereosinofilni sindrom
Bolniki s hudo astmo imajo lahko redko sistemski hipereozinofilni sindrom ali alergijski granulomatozni eozinofilni vaskulitis (Churg-Straussov sindrom), ki se običajno zdravita s sistemskimi kortikosteroidi.
V redkih primerih se lahko pri bolnikih, ki jemljejo zdravila proti astmi, vključno z omalizumabom, razvije ali razvije sistemska eozinofilija in vaskulitis. Ti dogodki so običajno povezani z zmanjšanjem peroralne terapije s kortikosteroidi.
Zdravnike je treba opozoriti, da se lahko pri takšnih bolnikih razvijejo izrazita eozinofilija, vaskulitični izpuščaj, poslabšanje pljučnih simptomov, nenormalnosti sinusov, srčni zapleti in / ali nevropatija.
V vseh hudih primerih z zgoraj omenjenimi motnjami imunskega sistema je treba razmisliti o prekinitvi zdravljenja z omalizumabom.
Parazitske okužbe (helminti)
IgE je lahko vključen v imunološki odziv na nekatere okužbe s helminti. Pri bolnikih s kronično visokim tveganjem za okužbo s helminti je s placebom nadzorovana študija pokazala rahlo povečanje stopnje okužbe z omalizumabom, čeprav na potek, resnost in odziv na zdravljenje okužbe to ni vplivalo. Na stopnjo okužbe to ni vplivalo. celoten klinični program, ki ni bil zasnovan za odkrivanje takšnih okužb, je bil manj kot 1 na 1.000 bolnikov, vendar je potrebna previdnost pri bolnikih z visokim tveganjem za okužbe s helminti, zlasti med potovanjem na območja, kjer so okužbe s helminti endemične. Če se bolniki ne odzovejo na priporočeno zdravljenje proti helmintom, je treba razmisliti o prekinitvi zdravljenja z zdravilom Xolair.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij -
Ker je lahko IgE vključen v imunološki odziv na nekatere okužbe s helminti, lahko zdravilo Xolair posredno zmanjša učinkovitost zdravil za zdravljenje helmintičnih ali drugih parazitskih okužb (glejte poglavje 4.4).
Encimi citokroma P450, iztočne črpalke in mehanizmi vezave beljakovin niso vključeni v očistek omalizumaba; zato je potencial medsebojnega delovanja med zdravili omejen. Študije medsebojnega delovanja zdravil ali cepiv niso bile izvedene. Xolair: Ni farmakoloških razlogov za pričakovanje tega običajno predpisana zdravila za astmo bodo delovala z omalizumabom.
V kliničnih preskušanjih se je zdravilo Xolair običajno uporabljalo v kombinaciji z inhalacijskimi in peroralnimi kortikosteroidi, inhalacijskimi kratkodelujočimi in dolgotrajnimi beta agonisti, antagonisti levkotriena, teofilinom in peroralnimi antihistaminiki. To ni nakazovalo. uporabljali zdravila proti astmi. Podatki o uporabi zdravila Xolair v kombinaciji s specifično imunoterapijo (hiposenzibilizirajoča terapija) so omejeni. V kliničnem preskušanju, kjer so zdravilo Xolair dajali hkrati z imunoterapijo, se varnost in učinkovitost zdravila Xolair v kombinaciji s specifično imunoterapijo nista razlikovali od tistih pri zdravilu Xolair. sam.
04.6 Nosečnost in dojenje -
Nosečnost
Podatkov o uporabi omalizumaba pri nosečnicah je malo. Študije na živalih ne kažejo neposrednih ali posrednih škodljivih učinkov na reproduktivno toksičnost (glejte poglavje 5.3). Omalizumab prehaja skozi placentno pregrado in potencialna škoda za plod ni bila povezano s starostno odvisnim zmanjšanjem števila trombocitov pri primatih razen človeka, z relativno večjo občutljivostjo pri mladoletnih živalih (glejte poglavje 5.3). Zdravila Xolair se med nosečnostjo ne sme uporabljati, razen če je to nujno potrebno.
Čas hranjenja
Ni znano, ali se omalizumab izloča v materino mleko pri ljudeh. Razpoložljivi podatki o primatih razen človeka so pokazali izločanje omalizumaba v mleko (glejte poglavje 5.3). Tveganja za novorojenčke / dojenčke ni mogoče izključiti. Omalizumaba se ne sme dajati med dojenjem.
Plodnost
Podatkov o plodnosti omalizumaba pri ljudeh ni. V nekliničnih študijah pri primatih razen človeka, posebej zasnovanih za oceno učinka na plodnost, vključno s študijami o parjenju, po večkratni uporabi omalizumaba niso opazili nobenih učinkov. do odmerkov 75 mg / kg Poleg tega v ločenih nekliničnih študijah genotoksičnosti niso opazili genotoksičnih učinkov (glejte poglavje 5.3).
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji -
Zdravilo Xolair nima vpliva ali ima zanemarljiv vpliv na sposobnost vožnje in upravljanja s stroji.
04.8 Neželeni učinki -
Povzetek varnostnega profila
Med kliničnimi preskušanji pri odraslih in mladostnikih, starih 12 let ali več, so bili najpogosteje poročani neželeni učinki reakcije na mestu injiciranja, vključno z bolečino, oteklino, eritemom in srbenjem ter glavobolom. V kliničnih preskušanjih pri otrocih od 6 do glavobola, vročine in bolečine v zgornjem delu trebuha. Večina reakcij je bila blagih ali zmernih.
Tabela neželenih učinkov
Tabela 4 navaja neželene učinke, zabeležene v kliničnih študijah pri celotni varnostni populaciji, zdravljeni z zdravilom Xolair, po klasifikaciji organskih sistemov MedDRA in pogostnosti. V vsakem razredu pogostnosti so neželeni učinki navedeni po padajoči resnosti.Pogostnosti so opredeljene kot: zelo pogosti (≥1 / 10), pogosti (≥1 / 100; v obdobju trženja so navedeni z neznanimi (pogostnosti ni mogoče oceniti iz razpoložljivih podatkov).
Preglednica 4: Neželeni učinki
*: zelo pogosto pri otrocih od 6
**: pri otrocih od 6
Opis izbranih neželenih učinkov
Motnje imunskega sistema
Za dodatne informacije glejte poglavje 4.4.
Arterijski trombembolični dogodki (ATE)
V kontroliranih kliničnih preskušanjih in med vmesnimi analizami opazovalne študije so opazili številčno neravnovesje arterijskih trombemboličnih dogodkov. Opredelitev sestavljene končne točke ATE je vključevala možgansko kap, prehodni ishemični napad, miokardni infarkt, nestabilno angino pektoris in srčno -žilno smrt (vključno s smrtjo iz neznanega vzroka). V končni analizi opazovalne študije je bila stopnja ATE na 1000 bolniških let 7, 52 (115 / 15.286 bolniških let) za bolnike, zdravljene z zdravilom Xolair, in 5,12 (51 / 9.963 bolniških let) za kontrolne bolnike. V "multivariatni kontrolni analizi izhodiščnih dejavnikov srčno-žilnega tveganja je bilo razmerje nevarnosti 1,32 (95% interval zaupanja 0,91-1,91). V novi združeni analizi kliničnega preskušanja, ki je vključevala vse v randomiziranih dvojno slepih, s placebom nadzorovanih študijah, ki so trajale 8 tednov ali več, je bila stopnja ATE na 1.000 bolniških let 2,69 (5 / 1.856 bolniških let) pri bolnikih, zdravljenih z zdravilom Xolair, in 2,38 (4 / 1.680 bolniških let) v skupini, ki je prejemala placebo (razmerje med stopnjami 1,13, 95% interval zaupanja 0,24-5,71) .
Trombociti
V kliničnih študijah je bilo pri nekaj bolnikih število trombocitov pod spodnjo mejo normalnega laboratorijskega območja. Nobena od teh sprememb ni bila povezana z epizodami krvavitve ali znižanim hemoglobinom. Pri ljudeh (bolniki, starejši od 6 let) niso poročali o vzorcih trajnega zmanjšanja števila trombocitov, na primer tistega, ki so ga opazili pri primatih razen človeka (glejte poglavje 5.3). v postmarketinških opazovanjih so poročali o posameznih primerih idiopatske trombocitopenije, vključno s hudimi primeri.
Parazitske okužbe
Pri bolnikih s kroničnim visokim tveganjem za okužbe s helminti je s placebom nadzorovana študija pokazala rahlo numerično povečanje stopnje okužbe v skupini bolnikov z omalizumabom, ki ni bilo statistično pomembno. Potek, resnost in odziv na zdravljenje okužb so ostali nespremenjeni (glejte poglavje 4.4).
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po registraciji zdravila, je pomembno, saj omogoča stalno spremljanje razmerja med koristmi in tveganji zdravila. Zdravstvene delavce prosimo, da o vsakem sumu na neželene učinke poročajo prek nacionalnega sistema poročanja.
04.9 Preveliko odmerjanje -
Največji dopustni odmerek zdravila Xolair ni bil določen. Bolnikom so dali enkratne intravenske odmerke do 4.000 mg brez dokazov o toksičnosti, ki omejuje odmerek. Največji kumulativni odmerek, ki je bil dan bolnikom, je bil 44.000 mg v obdobju 20 tednov in ta odmerek ni povzročil nobenih nepričakovanih akutnih učinkov.
Če obstaja sum na preveliko odmerjanje, je treba bolnika opazovati glede kakršnih koli nenormalnih znakov ali simptomov. Treba je poiskati ustrezno zdravljenje.
05.0 FARMAKOLOŠKE LASTNOSTI -
05.1 "Farmakodinamične lastnosti -
Farmakoterapevtska skupina: druga zdravila za sindrome obstruktivnih dihalnih poti za sistemsko uporabo, oznaka ATC: R03DX05
Omalizumab je humanizirano monoklonsko protitelo, pridobljeno iz rekombinantne DNK, ki se selektivno veže na humani imunoglobulin E (IgE). Protitelo je kapa IgG1, ki vsebuje humane podporne regije skupaj s komplementarno določevalnimi regijami mišjega protitelesa, ki se veže na IgE.
Mehanizem delovanja
Omalizumab se veže na IgE in preprečuje vezavo IgE na visoko afinitetni receptor FCεRI, s čimer se zmanjša količina prostega IgE, ki lahko sproži alergijsko kaskado. Pri atopičnih posameznikih zdravljenje z omalizumabom zmanjšuje tudi število receptorjev FCεRI, ki se nahajajo na bazofilih.
Farmakodinamični učinki
Sprostitev in vitro histamin iz bazofilcev, izoliranih pri osebah, zdravljenih z zdravilom Xolair, se je po stimulaciji z alergenom zmanjšal za približno 90% v primerjavi z vrednostmi pred zdravljenjem.
V kliničnih študijah so se ravni prostega IgE v serumu v eni uri po prvi uporabi znižale na odmerek in so ostale stabilne med odmerki. Eno leto po prekinitvi odmerjanja zdravila Xolair so se ravni IgE vrnile na raven pred zdravljenjem in po obdobju izločanja zdravila niso opazili povratnega učinka na ravni IgE.
Klinična učinkovitost in varnost
Odrasli in mladostniki, stari ≥ 12 let
Učinkovitost in varnost zdravila Xolair so dokazali v 28-tedenski dvojno slepi, s placebom kontrolirani študiji (študija 1), v kateri je sodelovalo 419 bolnikov s hudo alergijsko astmo, starih od 12 do 79 let, ki so imeli zmanjšano pljučno funkcijo (predviden FEV1 40-80%) in slab nadzor simptomov astme kljub zdravljenju z visokimi odmerki inhalacijskih kortikosteroidov in dolgotrajnim agonistom beta2. Upravičeni bolniki so imeli več astmatičnih poslabšanj, ki so zahtevala sistemsko zdravljenje s kortikosteroidi, ali pa so bili v preteklem letu zaradi hudega poslabšanja astme hospitalizirani ali odšli na urgenco, kljub nadaljevanju visokih odmerkov kortikosteroidov z inhalacijo in z dolgotrajnim agonistom beta2. Podkožni xolair ali placebo so kot dodatno terapijo dajali> 1.000 mikrogramov beklometazon dipropionata (ali enakovrednega) poleg dolgotrajnega agonista beta2. Vzdrževalne terapije s peroralnimi kortikosteroidi, teofilinom in antagonisti levkotrienov (22%, 27% in 35% bolnikov).
Primarni cilj je bila pogostnost poslabšanj astme, ki so zahtevala zdravljenje s sorazmerno visokimi odmerki sistemskih kortikosteroidov. Omalizumab je zmanjšal pogostnost poslabšanj astme za 19% (p = 0,153). Dodatne ocene, ki so pokazale statistično pomembnost (p
V analizi podskupine so bolniki s skupnim IgE ≥76 ie / ml pred zdravljenjem bolj verjetno dosegli klinično pomembne koristi z zdravilom Xolair. Pri teh bolnikih v študiji 1 je zdravilo Xolair zmanjšalo pogostnost poslabšanj astme za 40% (p = 0,002). dodatni bolniki v populaciji s skupnim IgE ≥76 ie / ml v programu Xolair pri hudi astmi so imeli klinično pomembne odzive. Tabela 5 vsebuje rezultate za celotno populacijo študije 1.
Tabela 5: Rezultati študije 1
* izrazito izboljšanje ali popoln nadzor
** p-vrednost za splošno porazdelitev vrednotenja
Študija 2 je ocenila učinkovitost in varnost zdravila Xolair pri populaciji 312 bolnikov s hudo alergijsko astmo, ki se je ujemala s populacijo študije 1. Zdravljenje z zdravilom Xolair v tej odprti študiji je povzročilo 61-odstotno zmanjšanje pogostnosti. Klinično pomembna poslabšanja astme v primerjavi s trenutno samo zdravljenje astme.
Štiri dodatne velike s placebom nadzorovane podporne študije, ki so trajale od 28 do 52 tednov pri 1722 odraslih in mladostnikih (študije 3, 4, 5, 6), so ovrednotile učinkovitost in varnost zdravila Xolair pri bolnikih s hudo dolgotrajno astmo. Nekateri bolniki niso bili ustrezno nadzorovani, vendar so v primerjavi s pacienti v študijah 1 ali 2. prejemali manj sočasnega zdravljenja astme. Študije 3-5 so kot primarni cilj uporabile poslabšanje, medtem ko so v študiji 6 pretežno ocenjevali zmanjšanje inhalacijskih kortikosteroidov.
V študijah 3, 4 in 5 se je pri bolnikih, zdravljenih z zdravilom Xolair, pogostnost poslabšanja astme zmanjšala za 37,5% (p = 0,027), 40,3% (p
V študiji 6 so znatno hujši bolniki z alergijsko astmo, zdravljeni z zdravilom Xolair, lahko znižali odmerek flutikazona na ≤500 mcg / dan brez poslabšanja nadzora astme (60,3%) v primerjavi s skupino s placebom (45,8%, p
Kakovost življenja so merili z vprašalnikom o kakovosti življenja, povezanem z brinovo astmo. V vseh šestih študijah je pri bolnikih z zdravilom Xolair prišlo do statistično pomembnega izboljšanja ocene kakovosti življenja v primerjavi s placebom ali kontrolnimi skupinami.
Splošna ocena učinkovitosti zdravljenja s strani zdravnika:
Zdravnikova splošna ocena je bila opravljena v petih zgoraj omenjenih študijah kot splošni ukrep nadzora astme, ki ga je izrazil zdravnik, ki je zdravil. Zdravnik je lahko upošteval največji pretok izdiha (PEF), dnevne in nočne simptome, uporabo zdravil za reševanje , spirometrija in poslabšanja. V vseh petih študijah je verjel, da je bistveno večji delež bolnikov, zdravljenih z zdravilom Xolair, dosegel izrazito izboljšanje ali popoln nadzor astme v primerjavi z bolniki, zdravljenimi s placebom.
Otroci od 6 do
Ključni podatki, ki podpirajo varnost in učinkovitost zdravila Xolair v obdobju od 6
Študija 7 je s placebom nadzorovana študija, ki je vključevala posebno podskupino (N = 235) bolnikov, kot je opredeljeno v tej indikaciji, zdravljenih z visokimi odmerki inhalacijskih kortikosteroidov (≥500 μg / dan flutikazona ali enakovrednega) poleg dolgotrajnega delovanja. beta-agonist.
Klinično pomembno poslabšanje je bilo v klinični presoji raziskovalca opredeljeno kot poslabšanje simptomov astme in je vključevalo podvojitev odmerka inhalacijskega kortikosteroida za vsaj 3 dni in / ali lajšanje sistemskih kortikosteroidov (peroralno ali intravensko) vsaj 3 dni.
V posebni podskupini bolnikov, ki so prejemali velike odmerke inhalacijskih kortikosteroidov, je bila stopnja poslabšanj astme v skupini, ki je prejemala omalizumab, bistveno nižja kot v skupini s placebom. zmanjšanje pri bolnikih, zdravljenih z omalizumabom, v primerjavi s placebom (razmerje v odstotkih 0,662, p = 0,047) .V drugem 28-tedenskem obdobju dvojno slepega zdravljenja je bila razlika med stopnjami poslabšanj v obeh zdravljenih skupinah 63-odstotno zmanjšanje za bolniki, zdravljeni z omalizumabom v primerjavi s placebom (razmerje v odstotkih 0,37, str
V 52. tednu dvojno slepega obdobja zdravljenja (ki obsega 24 tednov zdravljenja s fiksnim odmerkom steroidov in 28 tednov zdravljenja s spremenljivim odmerkom steroidov) je bila razlika v odstotkih med skupinami zdravljenja eno relativno zmanjšanje 50% (razmerje odstotkov 0,504, str
Ob koncu 52 tednov zdravljenja je skupina z omalizumabom pokazala večje zmanjšanje uporabe agonistov beta po potrebi kot skupina s placebom, čeprav razlika med obema skupinama zdravljenja ni bila statistično pomembna. konec 52-tedenskega dvojno slepega obdobja zdravljenja v podskupini hudih bolnikov z visokimi odmerki inhalacijskih kortikosteroidov v kombinaciji z dolgotrajnimi beta-agonisti je bil odstotek bolnikov z učinkovitostjo zdravljenja z oceno "odlično" višji, medtem ko je bil odstotek bolniki z učinkovitostjo zdravljenja z oceno "zmerno" ali "slabo" so bili v skupini, zdravljeni z omalizumabom, nižji kot v skupini, ki je prejemala placebo; razlika med obema skupinama je bila statistično pomembna (p
05.2 "Farmakokinetične lastnosti -
Farmakokinetiko omalizumaba so proučevali pri odraslih in mladostnikih z alergijsko astmo.
Absorpcija
Po podkožnem dajanju se omalizumab absorbira s povprečno absolutno biološko uporabnostjo 62%. Po subkutanem dajanju enkratnega odmerka pri odraslih in mladostnikih z astmo se je omalizumab počasi absorbiral in dosegel najvišjo serumsko koncentracijo po povprečnih 7-8 dneh. Farmakokinetika omalizumaba je linearna pri odmerkih nad 0,5 mg / kg. Po več odmerkih omalizumaba so bila območja v stanju dinamičnega ravnovesja pod krivuljo serumska koncentracija-čas od dneva 0 do dneva 14 do 6-krat večja od tistih, zabeleženih po prvem odmerku.
Dajanje zdravila Xolair v tekočih in liofiliziranih formulacijah je povzročilo podoben profil koncentracija-čas omalizumaba v serumu.
Distribucija
In vitro, omalizumab tvori majhne komplekse z IgE. Kompleksi padavin in kompleksi z molekulsko maso več kot milijon daltonov niso bili opaženi in vitro ali in vivo. Navidezni volumen porazdelitve pri bolnikih po subkutani uporabi je bil 78 ± 32 ml / kg.
Odprava
Odstranjevanje omalizumaba vključuje procese očistka IgG, pa tudi očistek s specifično vezavo in kompleksiranjem s svojim ciljnim ligandom, IgE. Izločanje IgG iz jeter vključuje razgradnjo v retikuloendotelnem sistemu in endotelijskih celicah. Nespremenjeni IgG se izloča tudi z žolčem. Pri bolnikih z astmo je razpolovni čas izločanja omalizumaba v serumu povprečno 26 dni s povprečnim navideznim očistkom 2,4 ± 1,1 ml / kg / dan. Poleg tega se je podvojitev telesne teže približno podvojila navidezni očistek.
Značilnosti pri populaciji bolnikov
Starost, rasa / narodnost, spol, indeks telesne mase
Za oceno učinkov demografskih značilnosti so analizirali populacijsko farmakokinetiko zdravila Xolair. Analize teh omejenih podatkov kažejo, da prilagoditev odmerka ni potrebna glede na starost (6-76 let), raso / narodnost, spol ali indeks telesne mase (glejte poglavje 4.2).
Ledvična in jetrna insuficienca
Farmakokinetičnih ali farmakodinamičnih podatkov pri bolnikih z okvaro ledvic ali jeter ni (glejte poglavji 4.2 in 4.4).
05.3 Predklinični podatki o varnosti -
Varnost omalizumaba so proučevali pri opicah cynomolgus, saj se omalizumab veže na cynomolgus in človeški IgE s podobno afiniteto. Protitelesa proti omalizumabu so bila najdena pri nekaterih opicah po večkratnem podkožnem ali intravenskem dajanju, vendar niso opazili očitne toksičnosti, kot je bolezen, ki jo povzroča imunski kompleks, ali od komplementa odvisna citotoksičnost. Anafilaktični odziv zaradi degranulacije mastocitov pri opicah cynomolgus.
Kronično dajanje omalizumaba do odmerkov 250 mg / kg (vsaj 14-kratni največji priporočeni klinični odmerek v mg / kg v skladu s preglednico priporočenih odmerkov) so dobro prenašali pri primatih razen človeka (odrasle in mladoletne živali), razen pri odmerkih in od starosti odvisnega zmanjšanja števila trombocitov z večjo občutljivostjo pri mladoletnih živalih. Koncentracija v serumu, ki je bila potrebna za doseganje 50% zmanjšanja trombocitov od izhodišča pri odraslih opicah cynomolgus, je bila približno 4 do 20-krat višja od pričakovane največje klinične serumske koncentracije Poleg tega so pri opicah cynomolgus opazili akutne krvavitve in vnetja na mestih injiciranja.
Uradnih študij rakotvornosti z omalizumabom niso izvedli.
V študijah razmnoževanja pri opicah cynomolgus podkožni odmerki do 75 mg / kg na teden (vsaj 8-kratni največji priporočeni klinični odmerek v mg / kg v 4-tedenskem obdobju) pri uporabi niso povzročili strupenosti za mater, zarodka ali teratogenosti. v celotnem obdobju organogeneze in pri dajanju v pozni nosečnosti, porodu in dojenju ni povzročil škodljivih učinkov na rast ploda ali novorojenčka.
Omalizumb se izloča v materino mleko opic cynomolgus. Koncentracije omalizumaba v mleku so bile 0,15% koncentracije v materinem serumu.
06.0 FARMACEVTSKE INFORMACIJE -
06.1 Pomožne snovi -
Prah
Saharoza
L-histidin
L-histidinijev klorid monohidrat
Polisorbat 20
Topilo
Voda za injekcije
06.2 Nezdružljivost "-
Tega zdravila ne smete mešati z drugimi zdravili, razen s tistimi, ki so omenjena v poglavju 6.6.
06.3 Obdobje veljavnosti "-
4 leta.
Po rekonstituciji
Kemična in fizikalna stabilnost rekonstituiranega zdravila je bila dokazana 8 ur pri 2 ° C do 8 ° C in 4 ure pri 30 ° C.
Z mikrobiološkega vidika je treba zdravilo uporabiti takoj po rekonstituciji. Če se ne uporabi takoj, je čas shranjevanja in pogoji shranjevanja pred uporabo odgovornost uporabnika in običajno ne smejo biti daljši od 8 ur pri 2 ° C - 8 ° C ali 2 uri pri 25 ° C.
06.4 Posebna navodila za shranjevanje -
Shranjujte v hladilniku (2 ° C - 8 ° C).
Ne zamrzujte.
Za pogoje shranjevanja po rekonstituciji glejte poglavje 6.3.
06.5 Vrsta neposredne embalaže in vsebina pakiranja -
Viala s praškom: prozorna, brezbarvna steklena viala tipa I z gumijastim zamaškom in sivim odpiralnim tesnilom.
Viala s topilom: prozorna, brezbarvna steklena viala tipa I, ki vsebuje 2 ml vode za injekcije.
Škatla, ki vsebuje eno vialo praška za raztopino za injiciranje in eno ampulo vode za injekcije.
06.6 Navodila za uporabo in ravnanje -
Liofilizirano zdravilo traja 15-20 minut, da se raztopi, čeprav včasih traja dlje. Popolnoma pripravljeno zdravilo je bistro ali rahlo neprozorno in ima lahko ob robu viale majhne mehurčke ali peno. Zaradi viskoznosti rekonstituiranega zdravila je treba pazljivo odstraniti ves izdelek iz viale, preden iz brizge iztisnemo odvečni zrak ali raztopino, da dobimo 0,6 ml.
Če želite pripraviti viale zdravila Xolair 75 mg za subkutano dajanje, sledite tem navodilom:
1. Iz viale potegnite 0,9 ml vode za injekcije v brizgo, opremljeno z veliko iglo velikosti 18.
2. Z vialo držite pokonci na ravni površini, vstavite iglo in vodo za injekcije prenesite v vialo, ki vsebuje liofiliziran prašek, po standardnih sterilnih tehnikah, tako da vodo za injekcije usmerite neposredno na prašek.
3. Vialo držite pokonci, večkrat močno obrnite (ne tresite) približno eno minuto, da se prašek enakomerno navlaži.
4. Za pomoč pri raztapljanju po končanem koraku 3 nežno obrnite vialo za 5-10 sekund, približno vsakih 5 minut, da se raztopijo preostali trdni delci.
Treba je omeniti, da lahko v nekaterih primerih traja več kot 20 minut, da se prah popolnoma raztopi. Če je tako, ponovite 4. korak, dokler v raztopini ni vidnih več gelastih delcev.
Ko se zdravilo popolnoma raztopi, v raztopini ne smejo biti vidni geli podobni delci. Majhni mehurčki ali pena okoli roba viale so pogosti. Rekonstituirano zdravilo bo videti bistro ali rahlo neprozorno. Ne uporabljajte, če so prisotni trdni delci.
5. Vialo obrnite vsaj 15 sekund, da raztopina steče v zamašek. Z novo 3 -ml brizgo, opremljeno z veliko iglo velikosti 18, vstavite iglo v vialo, obrnjeno navzdol. Vialo držite obrnjeno navzdol, pri vleku raztopine pazite, da konico igle postavite na dno raztopine v viali. brizgo. Preden iglo odstranite iz viale, bat povlecite do konca soda brizge, da izvlečete vso raztopino iz obrnjene viale.
6. Za podkožno injiciranje zamenjajte iglo velikosti 18 z iglo velikosti 25.
7. Izločite zrak, večje mehurčke in morebitno odvečno raztopino, da dobite zahtevano 0,6 ml raztopine. Na vrhu raztopine v brizgi lahko ostane tanka plast majhnih mehurčkov. Ker je raztopina rahlo viskozna, lahko dajanje raztopine z injekcijo pod kožo traja 5-10 sekund.
Viala daje 0,6 ml (75 mg) zdravila Xolair.
8. Injekcije se injicirajo subkutano v deltoidno področje roke ali stegna.
Xolair 75 mg prašek za raztopino za injiciranje je na voljo v viali za enkratno uporabo.
Z mikrobiološkega vidika je treba zdravilo uporabiti takoj po rekonstituciji (glejte poglavje 6.3).
Neuporabljeno zdravilo in odpadke, pridobljene iz tega zdravila, je treba odstraniti v skladu z lokalnimi predpisi.
07.0 IMETNIK "DOVOLJENJA ZA PROMET" -
Novartis Europharm Limited
Poslovni park Frimley
Camberley GU16 7SR
UK
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET -
EU/1/05/319/001
036892026
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA -
Datum prve odobritve: 25. oktober 2005
Datum zadnje obnove: 25. oktober 2010
10.0 DATUM REVIZIJE BESEDILA -
D.CCE junij 2015