Aktivne sestavine: Anidulafungin
ECALTA 100 mg prašek za koncentrat za raztopino za infundiranje
Indikacije Zakaj se uporablja zdravilo Ecalta? Za kaj je to?
Zdravilo ECALTA vsebuje zdravilno učinkovino anidulafungin in se uporablja pri odraslih za zdravljenje glivične okužbe krvi ali drugih notranjih organov, imenovane invazivna kandidiaza. Okužbo povzročajo celice vrste gliv (kvasovk), imenovane Candida.
Zdravilo ECALTA spada v skupino zdravil, imenovanih ehinokandini. Ta zdravila se uporabljajo za zdravljenje hudih glivičnih okužb.
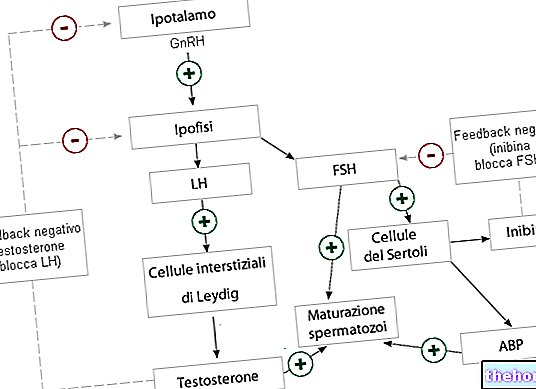
ECALTA preprečuje normalen razvoj glivičnih celičnih sten. V prisotnosti ECALTA imajo glivične celice nepopolne ali okvarjene celične stene, zaradi česar so krhke ali ne morejo rasti.
Kontraindikacije Kadar zdravila Ecalta ne smete uporabljati
Ne uporabljajte zdravila ECALTA:
- če ste alergični na anidulafungin, druge ehinokandine (npr. CANCIDAS) ali katero koli sestavino tega zdravila.
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Ecalta
Pred uporabo zdravila ECALTA se posvetujte z zdravnikom, farmacevtom ali medicinsko sestro, ki se bo morda odločila za spremljanje
- delovanje jeter bolj previdno, če se med zdravljenjem pojavijo težave z jetri.
- če ste med zdravljenjem z zdravilom ECALTA prejeli anestetike.
Otroci
Zdravila ECALTA se ne sme dajati bolnikom, mlajšim od 18 let.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Ecalta
Povejte svojemu zdravniku ali farmacevtu, če jemljete, ste pred kratkim jemali ali pa boste morda začeli jemati katero koli drugo zdravilo.
Ne začnite jemati drugih zdravil ali jih prenehajte uporabljati brez dovoljenja zdravnika ali farmacevta.
Opozorila Pomembno je vedeti, da:
Nosečnost in dojenje
Učinek zdravila ECALTA na nosečnice ni znan, zato uporaba zdravila ECALTA med nosečnostjo ni priporočljiva. Ženske v rodni dobi morajo uporabljati ustrezno metodo kontracepcije. Če med zdravljenjem z zdravilom ECALTA zanosite, se takoj posvetujte z zdravnikom.
Učinek zdravila ECALTA na doječe ženske ni znan. Pred uporabo se posvetujte z zdravnikom ali farmacevtom.
ECALTA med dojenjem. Preden vzamete katerokoli zdravilo, se posvetujte z zdravnikom ali farmacevtom.
Zdravilo ECALTA vsebuje fruktozo
To zdravilo vsebuje fruktozo (vrsto sladkorja). Če vam je zdravnik povedal, da ne prenašate nekaterih sladkorjev, se pred uporabo tega zdravila posvetujte z zdravnikom.
Odmerek, način in čas dajanja Kako uporabljati zdravilo Ecalta: Odmerjanje
Zdravilo ECALTA bo vedno pripravil in vodil zdravnik ali zdravstveni delavec (več informacij o načinu priprave tega zdravila boste našli na koncu navodila za uporabo v poglavju, namenjenem zdravnikom in zdravstvenim delavcem).
Zdravljenje se začne prvi dan z 200 mg (polnilni odmerek). Temu bo sledil dnevni odmerek 100 mg (vzdrževalni odmerek).
Zdravilo ECALTA se daje enkrat na dan s počasno (kapalno) infuzijo v veno. To bo trajalo najmanj 1,5 ure za vzdrževalni odmerek in 3 ure za polnilni odmerek.
Zdravnik bo določil trajanje zdravljenja in količino zdravila ECALTA, ki ga boste prejemali vsak dan, ter preveril vaš odziv na zdravljenje in vaše stanje.
Na splošno je treba zdravljenje nadaljevati vsaj 14 dni od zadnjega dne, ko so v krvi odkrili Candido.
Če ste pozabili uporabiti zdravilo ECALTA
Ker boste to zdravilo prejeli pod strogim zdravniškim nadzorom, je malo verjetno, da boste izpustili odmerek. Če menite, da ste izpustili odmerek, povejte svojemu zdravniku ali farmacevtu.
Zdravnik vam ne sme dati dvojnega odmerka.
Če ste prenehali jemati zdravilo ECALTA
Če vaš zdravnik preneha jemati zdravilo ECALTA, učinka ne sme biti.
Zdravnik vam lahko po zdravljenju z zdravilom ECALTA predpiše drugo zdravilo za nadaljevanje zdravljenja glivične okužbe ali za preprečitev njene ponovitve.
Če se prvotni simptomi okužbe ponovijo, o tem nemudoma obvestite svojega zdravnika ali drugega zdravstvenega delavca.
Če imate dodatna vprašanja o uporabi tega zdravila, se posvetujte z zdravnikom, farmacevtom ali medicinsko sestro.
Rekonstitucija
Vsako vialo je treba v aseptičnih pogojih rekonstituirati s 30 ml vode za injekcije, da dobimo koncentracijo 3,33 mg / ml. Čas priprave lahko traja do 5 minut. Po nadaljnjem redčenju je treba raztopino zavreči, če se ugotovi prisotnost delcev ali razbarvanje.
Rekonstituirano raztopino lahko shranite pri 25 ° C do 24 ur pred naslednjim redčenjem.
Redčenje in infuzija
Vsebino rekonstituirane viale je treba pod aseptičnimi pogoji prenesti v intravensko vrečko (ali plastenko), ki vsebuje natrijev klorid za infundiranje 9 mg / ml (0,9%) ali glukozo za infundiranje 50 mg / ml (5%), da dobimo koncentracija anidulafungina 0,77 mg / ml. Spodnja tabela prikazuje količine, potrebne za vsak odmerek.
Zahteve za redčenje za dajanje zdravila ECALTA
A: natrijev klorid za infundiranje 9 mg / ml (0,9%) ali glukoza za infundiranje 50 mg / ml (5%)
B: Koncentracija raztopine za infundiranje je 0,77 mg / ml. Hitrost infundiranja ne sme presegati 1,1 mg / min (kar ustreza 1,4 ml / min, če ste pripravljeni in razredčeni po navodilih).
Kadar koli dovoljujeta raztopina in vsebnik, je treba parenteralna zdravila pred dajanjem vizualno pregledati glede prisotnosti delcev ali razbarvanja.Če se ugotovi prisotnost delcev ali razbarvanje, je treba raztopino zavreči.
Samo za enkratno uporabo. Neuporabljeno zdravilo in odpadke, pridobljene iz tega zdravila, je treba odstraniti v skladu z lokalnimi predpisi.
Preveliko odmerjanje Kaj storiti, če ste vzeli preveč zdravila Ecalta
Če vas skrbi, da ste morda prejeli več zdravila ECALTA, kot bi smeli, nemudoma obvestite svojega zdravnika ali drugega zdravstvenega delavca.
Neželeni učinki Kakšni so stranski učinki zdravila Ecalta
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih. Nekatere od teh neželenih učinkov bo opazil vaš zdravnik, ko bo spremljal vaš odziv in stanje.
Med zdravljenjem z zdravilom ECALTA so redko poročali o smrtno nevarnih alergijskih reakcijah, vključno s težavami pri dihanju s piskanjem ali poslabšanjem že obstoječih izpuščajev.
Resni neželeni učinki - takoj obvestite svojega zdravnika ali drugega zdravstvenega delavca, če opazite kaj od naslednjega:
- Krči (krči)
- Rdečica
- Kožni izpuščaj, srbenje
- Vročinski oblivi
- Urtikarija
- Nenadna kontrakcija mišic dihalnih poti, ki lahko povzroči piskanje ali kašelj
- Težave pri dihanju
Drugi stranski učinki
Zelo pogosti neželeni učinki (pojavijo se lahko pri več kot 1 od 10 bolnikov) so:
- Nizke ravni kalija v krvi (hipokaliemija)
- Driska
- Slabost
Pogosti neželeni učinki (pojavijo se lahko pri največ 1 od 10 bolnikov) so:
- Krči (krči)
- Glavobol
- Umaknil se je
- Spremembe testov delovanja jeter
- Kožni izpuščaj, srbenje
- Spremembe testov delovanja ledvic
- Sprememba pretoka žolča iz žolčnika v črevo (holestaza)
- Visoka raven sladkorja v krvi
- Visok krvni pritisk
- Nizek krvni tlak
- Nenadna kontrakcija mišic dihalnih poti, ki lahko povzroči piskanje ali kašelj
- Težave pri dihanju
Občasni neželeni učinki (pojavijo se lahko pri največ 1 od 100 bolnikov) so:
- Motnje strjevanja krvi
- Rdečica
- Vročinski oblivi
- Bolečina v trebuhu
- Urtikarija
- Bolečina na mestu injiciranja
Neželeni učinki neznane pogostosti (pogostnosti iz razpoložljivih podatkov ni mogoče oceniti) so:
- Alergijske reakcije, ki so smrtno nevarne
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom, farmacevtom ali medicinsko sestro.To vključuje vse možne neželene učinke, ki niso navedeni v tem navodilu. za več informacij o varnosti tega zdravila.
Potek in zadržanje
Zdravilo shranjujte nedosegljivo otrokom! Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na nalepki.
Shranjujte v hladilniku (2 ° C - 8 ° C).
Pripravljeno raztopino lahko shranite pri 25 ° C do 24 ur. Raztopino za infundiranje lahko shranite pri 25 ° C (sobna temperatura) do 48 ur ali zamrznjeno vsaj 72 ur in jo dajte pri 25 ° C (sobna temperatura) v 48 urah.
Ne zavrzite nobenih zdravil v odpadno vodo ali med gospodinjske odpadke.
Druge informacije
Kaj vsebuje zdravilo ECALTA
Zdravilna učinkovina je anidulafungin. Ena viala s praškom vsebuje 100 mg anidulafungina
Pomožne snovi so: fruktoza, manitol, polisorbat 80, vinska kislina, natrijev hidroksid (za uravnavanje pH), klorovodikova kislina (za uravnavanje pH).
Izgled zdravila ECALTA in vsebina pakiranja
Zdravilo ECALTA je na voljo v pakiranju, ki vsebuje 1 vialo s 100 mg praška za koncentrat za raztopino za infundiranje.
Prašek je bel do sivobel.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA
ECALTA 100 mg prah za koncentrat za raztopino za infuzijo
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA
Ena viala vsebuje 100 mg anidulafungina.
Rekonstituirana raztopina vsebuje 3,33 mg / ml anidulafungina, razredčena raztopina pa 0,77 mg / ml anidulafungina.
Pomožna snov z znanimi učinki: fruktoza 102,5 mg na vialo.
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA
Prašek za koncentrat za raztopino za infundiranje.
Bel do sivobel trden liofilizat.
Rekonstituirana raztopina ima pH od 3,5 do 5,5.
04.0 KLINIČNE INFORMACIJE
04.1 Terapevtske indikacije
Zdravljenje invazivne kandidiaze pri odraslih bolnikih (glejte poglavji 4.4 in 5.1).
04.2 Odmerjanje in način uporabe
Zdravljenje z zdravilom ECALTA mora uvesti zdravnik z izkušnjami pri zdravljenju invazivnih glivičnih okužb. Vzorce glivičnih kultur je treba zbrati pred začetkom zdravljenja.Terapijo lahko začnemo, preden so znani rezultati preskusov kulture, in jih lahko ustrezno prilagodimo, ko bodo ti rezultati na voljo.
Odmerjanje
Prvi dan zdravljenja je treba dati en sam polnilni odmerek 200 mg, nato pa 100 mg na dan. Trajanje zdravljenja mora temeljiti na bolnikovem kliničnem odzivu. Na splošno je treba protiglivično terapijo nadaljevati vsaj 14 dni po zadnji pozitivni kulturi.
Trajanje zdravljenja
Ni dovolj podatkov, ki bi podpirali uporabo 100 -miligramskega odmerka za obdobje zdravljenja, daljše od 35 dni.
Bolniki z okvaro ledvic in jeter
Pri bolnikih z blago, zmerno ali hudo okvaro jeter prilagoditev odmerka ni potrebna. Pri bolnikih z okvaro ledvic, vključno z bolniki na dializi, prilagoditev odmerka ni potrebna. Zdravilo ECALTA se lahko daje ne glede na to, kdaj se izvaja dializa (glejte poglavje 5.2).
Druge posebne populacije bolnikov
Pri odraslih bolnikih prilagoditev odmerka ni potrebna glede na spol, težo, narodnost, pozitivnost na HIV ali pri starejših bolnikih (glejte poglavje 5.2).
Pediatrična populacija
Varnost in učinkovitost zdravila ECALTA pri otrocih, mlajših od 18 let, nista bili ugotovljeni, trenutno razpoložljivi podatki so opisani v poglavju 5.2, vendar priporočenega režima ni mogoče razbrati.
Način dajanja
Samo za intravensko dajanje.
Zdravilo ECALTA je treba rekonstituirati z vodo za injekcije v koncentraciji 3,33 mg / ml in nato razredčiti do koncentracije 0,77 mg / ml. Za navodila o rekonstituciji zdravila pred uporabo glejte poglavje 6.6.
Priporočljivo je, da zdravilo ECALTA dajete s hitrostjo infundiranja, ki ne presega 1,1 mg / min (kar ustreza 1,4 ml / min, ko je prašek rekonstituiran in razredčen po navodilih). Reakcije, povezane z infuzijo, so redke, če hitrost infundiranja anidulafungina ne presega 1,1 mg / min (glejte poglavje 4.4).
Zdravila ECALTA se ne sme dajati kot bolus.
04.3 Kontraindikacije
Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov, navedeno v poglavju 6.1.
Preobčutljivost za druga zdravila razreda ehinokandin.
04.4 Posebna opozorila in ustrezni previdnostni ukrepi za uporabo
Zdravila ECALTA niso preučevali pri bolnikih z endokarditisom, osteomielitisom ali meningitisom Candida.
Učinkovitost zdravila ECALTA so ocenjevali le pri omejenem številu bolnikov z nevtropenijo (glejte poglavje 5.1).
Jetrni učinki
Pri zdravih osebah in pri bolnikih, zdravljenih z anidulafunginom, so opazili zvišanje ravni jetrnih encimov. Klinično pomembne spremembe v jetrih so se pojavile pri nekaterih bolnikih z resnimi osnovnimi boleznimi, ki so se zdravili z več sočasnimi zdravili skupaj z anidulafunginom. V kliničnih študijah so bile epizode hude jetrne disfunkcije, hepatitisa in odpovedi jeter redke. Bolnike z zvišanjem jetrnih encimov med zdravljenjem z anidulafunginom je treba spremljati glede možnega poslabšanja delovanja jeter in oceniti razmerje med tveganji in koristmi pri nadaljevanju zdravljenja z anidulafunginom.
Anafilaktične reakcije
Med uporabo anidulafungina so poročali o anafilaktičnih reakcijah, vključno s šokom.
Reakcije, povezane z infuzijo
Med zdravljenjem z anidulafunginom so poročali o neželenih učinkih, povezanih z infuzijo, vključno z izpuščajem, urtikarijo, zardevanjem, srbenjem, dispnejo, bronhospazmom in hipotenzijo.
V neklinični študiji (pri podganah) so opazili poslabšanje z infuzijo povezanih reakcij (glejte poglavje 5.3). Klinični pomen tega učinka ni znan. Vendar je potrebna previdnost pri sočasni uporabi anidulafungina in anestetiki.
Vsebnost fruktoze
Bolniki z redko dedno intoleranco za fruktozo ne smejo jemati tega zdravila.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij
Anidulafungin ni klinično pomemben substrat, induktor ali zaviralec izoencimov citokroma P450 (1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 3A). Pomembno je poudariti, da študije v vitro ne izključujejo v celoti možnosti interakcij in vivo.
Študije medsebojnega delovanja so bile opravljene z anidulafunginom in drugimi zdravili, pri katerih je verjetnost sočasne uporabe. Pri uporabi teh zdravil skupaj s ciklosporinom, vorikonazolom in takrolimusom ni priporočljivo prilagajanja odmerka teh zdravil ali anidulafungina, pri sočasni uporabi z amfotericinom B ali rifampicinom pa prilagoditev odmerka anidulafungina ni priporočljiva.
Pediatrična populacija
Študije interakcij so bile izvedene samo pri odraslih.
04.6 Nosečnost in dojenje
Nosečnost
Ni zadostnih podatkov o uporabi anidulafungina pri nosečnicah.
Pri kuncih, zdravljenih z andidulafunginom med nosečnostjo v prisotnosti strupenosti za mater, so opazili blage razvojne učinke (glejte poglavje 5.3). Možno tveganje za ljudi ni znano. Zato uporaba anidulafungina med nosečnostjo ni priporočljiva.
Čas hranjenja
Študije na živalih so pokazale, da se anidulafungin izloča v materino mleko. Ni znano, ali se anidulafungin izloča v materino mleko pri ljudeh. Odločiti se, ali naj nadaljuje / prekiniti dojenje ali zdravljenje z anidulafunginom, je treba ob upoštevanju koristi dojenja za otroka in koristi zdravljenja z anidulafunginom za mamo.
Plodnost
V študijah pri samcih in samicah podgan pri anidulafunginu niso opazili vpliva na plodnost (glejte poglavje 5.3).
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji
Študije o sposobnosti vožnje in upravljanja s stroji niso bile izvedene.
04.8 Neželeni učinki
Povzetek varnostnega profila
Petsto petinšestdeset pet oseb je bilo v kliničnih preskušanjih zdravljenih z enkratnimi ali večkratnimi odmerki anidulafungina v veni: 1308 bolnikov v kliničnih preskušanjih faze 2/3 (923 bolnikov z invazivno kandidozo / kandidiazo, 355 bolnikov z oralno / požiralno kandidiazo, 30 bolnikov z invazivna aspergiloza) in 257 bolnikov v študijah prve faze.
Varnostni profil anidulafungina temelji na 840 bolnikih z invazivno kandidemijo / kandidiazo, zdravljenih s priporočenim dnevnim odmerkom 100 mg v 9 študijah. Sprva v treh študijah (ena primerjalna proti flukonazol, dva neprimerljiva) 204 bolnikov je bilo pregledanih; povprečno trajanje intravenskega zdravljenja pri teh bolnikih je bilo 13,5 dni (razpon od 1 do 38 dni), 119 bolnikov pa je bilo ≥ 14 dni zdravljenih z anidulafunginom. V 6 drugih študijah (dve primerjalni proti kaspofungin in štirje neprimerljivi), je bilo pregledanih 636 bolnikov, od tega 53 nevtropeničnih in 131 z okužbo globokega tkiva; povprečno trajanje intravenskega zdravljenja pri bolnikih z nevtropenijo in pri bolnikih z okužbo globokih tkiv v teh študijah je bilo 10,0 (razpon 1 do 42) oziroma 14,0 (razpon 1 do 42) dni. Neželeni učinki so bili na splošno blagi do zmerni in so redko vodili do prekinitve zdravljenja.
Med zdravljenjem z anidulafunginom so v kliničnih preskušanjih poročali o neželenih učinkih, povezanih z infuzijo, kot je povzeto v preglednici 1, kot so: zardevanje, zardevanje, pruritus, izpuščaj in urtikarija.
Tabelirani neželeni učinki
Spodnja tabela vključuje neželene učinke vseh vzrokov (izrazi MedDRA), opažene pri 840 preiskovancih, zdravljenih s 100 mg anidulafungina z ustrezno pogostostjo, zelo pogosti (≥ 1/10), pogosti (≥ 1/100 do
Tabela 1. Tabela neželenih učinkov
* Glejte poglavje 4.4.
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po odobritvi zdravila, je pomembno, saj omogoča stalno spremljanje razmerja med koristmi in tveganji zdravila. Zdravstvene delavce prosimo, da o vsakem sumu na neželene učinke poročajo prek nacionalnega sistema za poročanje. V "Prilogi V .
04.9 Preveliko odmerjanje
Kot pri vsakem prevelikem odmerjanju je treba uporabiti potrebne splošne podporne ukrepe.
V primeru prevelikega odmerjanja se lahko pojavijo neželeni učinki, navedeni v poglavju 4.8.
V kliničnih preskušanjih so enkratni odmerek 400 mg anidulafungina nehote dali kot polnilni odmerek. O neželenih učinkih niso poročali. V študiji, v kateri je sodelovalo 10 zdravih prostovoljcev, niso opazili toksičnosti, ki bi omejevala odmerek. mg na dan; 3 od 10 preiskovancev je poročalo o prehodnem in asimptomatskem povečanju transaminaz (≤ 3 x zgornja normalna meja (ULN)).
ECALTA ni za dializo.
05.0 FARMAKOLOŠKE LASTNOSTI
05.1 Farmakodinamične lastnosti
Farmakoterapevtska skupina: protiglivična sredstva za sistemsko uporabo, druga protiglivična sredstva za sistemsko uporabo.
Oznaka ATC: JO2AX06.
Mehanizem delovanja
Anidulafungin je "polsintetični ehinokandin, lipopeptid, sintetiziran iz produkta fermentacije"Aspergillus nidulans.
Anidulafungin selektivno zavira encim beta-D-glukan-sintazo, ki ga najdemo v glivičnih celicah, vendar ne v celicah sesalcev. To vključuje "zaviranje tvorbe beta-D-glukana, bistvene sestavine celične stene gliv. Anidulafungin je pokazal" fungicidno delovanje proti Candida spp. in "aktivnost proti območjem aktivne celične rasti hif Aspergillus fumigatus.
Dejavnosti in vitro
Anidulafungin je pokazal "aktivnost" in vitro proti C. albicans, C. glabrata, C. parapsiloza, C. krusei In C. tropicalis. Za klinični pomen teh podatkov glejte "Klinična učinkovitost in varnost" Aspergillus fumigatus.
Izolati z mutacijami v vročih točkah ciljnega gena so bili povezani s kliničnimi napakami ali novimi nastopi glivičnih okužb (preboj). V večini kliničnih primerov je zdravljenje s kaspofunginom vključeno. Vendar pa v poskusih na živalih te mutacije dajejo navzkrižno odpornost na vse tri ehinokandine, zato se ti izolati, dokler se ne pridobijo nadaljnje klinične izkušnje z anidulafunginom, razvrstijo kot odporne na ehinokandine.
Dejavnost in vitro anidulafungina proti vrsti Candida ni enotna. Natančneje, za C. parapsiloza MIC (minimalne inhibitorne koncentracije) anidulafungina so višje kot pri drugih vrstah Candida. "Evropski odbor za testiranje občutljivosti na protimikrobna zdravila (EUCAST) je opredelil standardizirano tehniko za test občutljivosti vrst na anidulafungin Candida pa tudi ustrezne razlagalne meje.
Tabela 2. Prelomne točke EUCAST
1 C. parapsiloza ima "bistveno spremembo v ciljnem genu, ki je verjetno mehanizem, odgovoren za višje MIC kot druge vrste Candida. V kliničnih študijah je izid anidulafungina s C. parapsiloza vendar se uporaba ehinokandinov pri kandidemiji ni statistično razlikovala od drugih vrst C. parapsiloza morda ne velja za terapijo prve izbire
2 EUCAST ni določil mejnih vrednosti za anidulafungin, ki niso povezane z vrsto
Dejavnosti in vivo
Parenteralno dani anidulafungin je bil učinkovit proti vrstam Candida v imunokompetentnih in imunsko oslabljenih modelih miši in zajcev. Zdravljenje z anidulafunginom je podaljšalo stopnjo preživetja in tudi zmanjšalo breme Candida spp. v zadevnem organu, če se določi v presledkih med 24 in 96 urami od zadnjega zdravljenja.
Okužbe, preučene pri laboratorijskih živalih, so vključevale razširjeno okužbo C. albicans pri nevtropeničnih kuncih okužba požiralnika / orofaringeusa pri nevtropeničnih kuncih z C. albicans odporne na flukonazol in diseminirano okužbo nevtropenične miši z okužbami C. glabrata odporen na flukonazol.
Klinična učinkovitost in varnost
Kandidemija in druge oblike invazivne kandidoze
Varnost in učinkovitost anidulafungina so ocenjevali v osrednjem, randomiziranem, dvojno slepem, multicentričnem kliničnem preskušanju 3. faze, ki je bilo izvedeno v več državah pri bolnikih, ki niso bili nevtropenični, s kandidemijo in pri omejenem številu bolnikov z globoko zakoreninjenimi okužbami. Candida lokaliziran v tkivih ali povezan z nastankom abscesov. Bolniki z endokarditisom, osteomielitisom ali meningitisom iz Candidaali tisti z okužbami iz C. krusei, so bili posebej izključeni iz študije. Bolniki so bili naključno izbrani za prejemanje anidulafungina (200 mg intravenskega polnilnega odmerka, ki mu je sledilo 100 mg na dan intravensko) ali flukonazola (800 mg intravenskega nakladalnega odmerka, ki mu je sledilo 400 mg na dan) in so bili stratificirani po lestvici APACHE II (≤ 20 in> 20) in na podlagi prisotnosti ali odsotnosti nevtropenije. Zdravljenje je trajalo najmanj 14 dni in največ 42 dni. Bolniki v obeh skupinah zdravljenja so po najmanj 10 dneh intravenskega zdravljenja lahko prešli na peroralni flukonazol, če so prenašali peroralno zdravljenje in so bili vsaj 24 ur afebrilni in so bile novejše krvne kulture negativne za Candida spp.
Bolniki, ki so prejeli vsaj en odmerek študijskega zdravila in so imeli pozitivno kulturo Candida spp. z normalno sterilnega mesta pred vključitvijo v študijo. opredeljena dvostopenjska statistična primerjava (neinferiornost, ki ji sledi superiornost). Uspešen celoten odziv je zahteval klinično izboljšanje in mikrobiološko izkoreninjenje. Bolnike so spremljali šest tednov po zaključku celotne terapije.
Dvesto petinpetdeset bolnikov, starih od 16 do 91 let, je bilo naključno izbranih za zdravljenje in prejelo vsaj en odmerek študijskega zdravila. Najpogosteje izolirane vrste ob izletu so bile C. albicans (63,8% anidulafungina, 59,3% flukonazola), sledi C. glabrata (15,7 %, 25,4 %), C. parapsiloza (10,2%, 13,6%) e C. tropicalis (11,8%, 9,3%) - z 20, 13 in 15 sevi zadnjih 3 vrst v skupini anidulafunginov. Večina bolnikov je imela oceno APACHE II ≤ 20, zelo majhno število pa je bilo nevtropeničnih.
Podatki o učinkovitosti, globalni in povezani z različnimi podskupinami, so prikazani spodaj v tabeli 3.
a Izračunano kot anidulafungin minus flukonazol
b S sočasno kandidemijo ali brez nje
c Intraabdominalno
d Podatki za bolnike z enim samim patogenom na začetku
in 98,3% intervali zaupanja za večkratne primerjave, opravljene v poznejših časih s post-hoc analizo.
Stopnje umrljivosti v obeh skupinah zdravljenja z anidulafunginom in flukonazolom so prikazane spodaj v preglednici 4:
Dodatni podatki pri bolnikih z nevtropenijo
Učinkovitost anidulafungina (200 mg intravenskega polnilnega odmerka, ki mu sledi 100 mg na dan intravensko) pri odraslih bolnikih z nevtropenijo (opredeljeno z absolutnim številom nevtrofilcev ≤ 500 celic / mm3, beločnicami ≤ 500 celic / mm3 ali raziskovalcem, ki je bil na začetku opredeljen kot nevtropeničen) mikrobiološko potrjeno invazivno kandidozo so ovrednotili v "združeni analizi 5 prospektivnih študij (1 primerjalna proti kaspofungin in 4 odprti, neprimerljivi). Bolnike so zdravili najmanj 14 dni. Pri klinično stabilnih bolnikih je bil prehod na peroralno zdravljenje z azolom dovoljen po vsaj 5-10 dneh zdravljenja z anidulafunginom. V analizo je bilo vključenih 46 bolnikov. Večina bolnikov je imela samo kandidemijo (84,8%; 39/46). Na začetku so bili najpogosteje izolirani patogeni C. tropicalis (34,8%; 16/46), C. krusei (19,6%; 9/46), C. parapsiloza (17,4%; 8/46), C. albicans (15,2%; 7/46) in C. glabrata (15,2%; 7/46). Skupna stopnja odziva na uspeh intravenskega zdravljenja (primarni cilj) je bila 26/46 (56,5%), na koncu vseh zdravljenj pa 24/46 (52,2%). Umrljivost vseh vzrokov do konca študije (6-tedenski kontrolni obisk) je bila 21/46 (45,7%).
Učinkovitost anidulafungina pri odraslih bolnikih z nevtropenijo (določeno z absolutnim številom nevtrofilcev ≤ 500 celic / mm3 na začetku) z invazivno kandidiazo je bila ocenjena v prospektivni, kontrolirani, dvojno slepi, randomizirani študiji.Upravičeni bolniki so bili zdravljeni z anidulafunginom (200 mg intravenski nakladalni odmerek, ki mu je sledilo 100 mg na dan intravensko) ali kaspofunginom (70 mg intravenski polnilni odmerek, ki mu je nato sledilo 50 mg na dan intravensko.) (Randomizacija 2: 1). Bolnike so zdravili najmanj 14 dni.
Pri klinično stabilnih bolnikih je bil prehod na peroralno zdravljenje z azolom dovoljen po vsaj 10 dneh študijskega zdravljenja. V študijo je bilo vključenih 14 bolnikov z nevtropenijo z mikrobiološko potrjeno invazivno kandidozo (populacija MITT) (11 anidulafungina, kaspofungina). Večina bolnikov je imela samo kandidemijo. Najpogosteje so bili na začetku izolirani patogeni C. tropicalis (4 anidulafungin, 0 kaspofungin), C.. parapsiloza (2 anidulafungina, 1 kaspofungin), C. krusei (2 anidulafungina, 1 kaspofungin) C. ciferrii (2 anidulafungina, 0 kaspofungina). Skupna stopnja uspešnega odziva na koncu intravenskega zdravljenja (primarni cilj) je bila 8/11 (72,7%) za anidulafungin in 3/3 (100%) za kaspofungin (razlika -27,3, 95%IZ: -80,9, 40,3); skupna stopnja uspešnosti odziva na koncu vseh zdravljenj je bila 8/11 (72,7%) za anidulafungin in 3/100%) za kaspofungin (razlika -27,3, 95%IZ: -80, 9, 40,3). Vse do 6-tedenskega kontrolnega obiska za anidulafungin (populacija MITT) je bila vsa smrtnost zaradi vzrokov 4/11 (36,4%) in 2/3 (66,7%) za kaspofungin.
Bolniki z mikrobiološko potrjeno invazivno kandidiazo (populacija MITT) in nevtropenijo so bili ugotovljeni v "združeni analizi 4 podobno zasnovanih, odprtih, neprimerljivih prospektivnih študij. Učinkovitost anidulafungina (200 mg polnilni odmerek na intravensko, sledi 100 mg na dan intravensko) je bila ovrednotena pri 35 definiranih nevtropeničnih odraslih bolnikih z absolutnim številom nevtrofilcev ≤ 500 celic / mm3 ali pri 22 bolnikih z belimi krvničkami ≤ 500 celic / mm3 ali pri 13 bolnikih, ki so jih na podlagi raziskav razvrstili kot nevtropenične na začetku. Bolnike so zdravili najmanj 14 dni. Pri klinično stabilnih bolnikih je bil prehod na peroralno zdravljenje z azolom dovoljen po vsaj 5-10 dneh zdravljenja z anidulafunginom. Večina bolnikov je imela samo kandidemijo (85,7%). Najpogosteje so bili na začetku izolirani patogeni C. tropicalis (12 bolnikov), C. albicans (7 bolnikov), C. glabrata (7 bolnikov), C. krusei (7 bolnikov) e C. parapsiloza (6 bolnikov). Skupna stopnja uspešnega odziva na koncu intravenskega zdravljenja (primarni cilj) je bila 18/35 (51,4%) in 16/35 (45,7%) na koncu vseh zdravljenj. Smrtnost vseh vzrokov na 28. dan je bila 10/35 (28,6%). Skupna stopnja uspešnosti odziva na koncu intravenskega zdravljenja in na koncu vseh zdravljenj je bila 7/13 (53,8%) za oba od 13 bolnikov, ki jih je preiskovalec na začetku uvrstil med nevtropenične.
Dodatni podatki pri bolnikih z okužbami globokih tkiv
Učinkovitost anidulafungina (200 mg intravenskega nakladalnega odmerka, ki mu sledi 100 mg na dan intravensko) pri odraslih bolnikih z mikrobiološko potrjeno globoko tkivno kandidiazo so ocenili v združeni analizi 5 prospektivnih študij s podobno zasnovo (1 primerjalna in 4 odprte). Bolnike so zdravili najmanj 14 dni. V štirih odprtih študijah je bil prehod na peroralno zdravljenje z azolom dovoljen po vsaj 5-10 dneh zdravljenja z anidulafunginom. V analizo je bilo vključenih 129 bolnikov. Enaindvajset bolnikov (16,3%) je imelo sočasno kandidemijo. Povprečna ocena APACHE II je bila 14,9 (razpon 2-44). Najpogostejša mesta okužbe so bile peritonealna votlina 54,3%, 70/129), hepatobiliarni trakt (7,0%, 9/129), plevralna votlina (5,4%, 7/129) in ledvice (3,1%, 4/129) Na začetku so bili najpogosteje izolirani patogeni iz globokega tkiva C. albicans (64,3%; 83/129), C. glabrata (31,0%; 40/129), C. tropicalis (11,6%; 15/129) e C. krusei (5,4%; 7/129). Tabela 5 poroča o splošni stopnji uspešnosti ob koncu intravenskega zdravljenja (primarni cilj) in na koncu vseh zdravljenj ter o smrtnosti zaradi vseh vzrokov do 6-tedenskega kontrolnega obiska.
a Celoten odziv na uspeh je bil opredeljen kot klinični in mikrobiološki uspeh
b EOIVT, Konec intravenskega zdravljenja; EOT, Konec vsega zdravljenja
05.2 Farmakokinetične lastnosti
Splošne značilnosti farmakokinetike
Farmakokinetiko anidulafungina so opredelili pri zdravih prostovoljcih, pri posebnih populacijah in pri bolnikih. Pri sistemski izpostavljenosti so opazili nizko variabilnost med subjekti (koeficient variacije? 25%) stanje dinamičnega ravnovesja je bil dosežen prvi dan po polnilnem odmerku (dvakratni vzdrževalni odmerek).
Distribucija
Za farmakokinetiko anidulafungina je značilna hitra razpolovna doba porazdelitve (0,5-1 ura) in volumen porazdelitve 30-50 L, kar je podobno prostornini celotne telesne tekočine.
Anidulafungin se v veliki meri (> 99%) veže na beljakovine v plazmi. Posebne študije o porazdelitvi anidulafungina v tkivih pri ljudeh niso bile izvedene, zato ni na voljo podatkov o prodiranju anidulafungina v cerebrospinalno tekočino (CSF) in / ali skozi krvno-možgansko pregrado.
Biotransformacija
Jetrna presnova anidulafungina ni bila opažena. Anidulafungin ni klinično pomemben substrat, induktor ali zaviralec izoencimov citokroma P450. Ni verjetno, da bi imel anidulafungin klinično pomembne učinke na presnovo zdravil, ki se presnavljajo z izoencimi citokroma P450.
Anidulafungin se s počasno kemično razgradnjo pri fizioloških temperaturah in pH pretvori v peptid z odprto zanko brez protiglivičnega delovanja. Razpolovna doba razgradnje in vitro anidulafungina v fizioloških pogojih je približno 24 ur. Izdelek z odprto zanko in vivonato se pretvori v sredstva za razgradnjo peptidov in se izloči predvsem z izločanjem z žolčem.
Odprava
Očistek anidulafungina je približno 1 l / h. Anidulafungin ima pretežni razpolovni čas izločanja približno 24 ur, kar je značilno za večino profila koncentracije v času v plazmi in končni razpolovni čas 40-50 ur, ki je značilen za končno fazo izločanja profila.
V klinični študiji z enim odmerkom so zdrave prostovoljce dajali radioaktivno označen (14C) anidulafungin (≥ 88 mg). Približno 30% danega radioaktivnega odmerka se je izločilo v blatu v 9 dneh, manj kot 10% odmerka pa se je izločilo kot nespremenjeno zdravilo. Manj kot 1% danega radioaktivnega odmerka se je izločilo z urinom, kar kaže na zanemarljiv ledvični očistek . Koncentracije anidulafungina so 6 dni po dajanju padle pod spodnje meje količinske opredelitve. V krvi, urinu in blatu so bile 8 tednov po dajanju zanemarljive količine radioaktivnosti, pridobljene z zdravilom.
Linearnost
Anidulafungin ima linearno farmakokinetiko v širokem razponu enkratnih dnevnih odmerkov (15-130 mg).
Posebne populacije bolnikov
Bolniki z glivičnimi okužbami
Farmakokinetika anidulafungina pri bolnikih z glivičnimi okužbami je podobna tisti pri zdravih osebah na podlagi populacijskih farmakokinetičnih analiz. Pri dnevnem režimu odmerjanja 200/100 mg pri hitrosti infundiranja 1,1 mg / min je Cmax pri stanje dinamičnega ravnovesja in najnižje koncentracije (Cmin) so dosegle 7 oziroma 3 mg / l, s povprečno AUC pri stanje dinamičnega ravnovesja približno 110 mg • h / l.
Utež
Čeprav je bila s populacijsko farmakokinetično analizo teža ugotovljena kot vir variabilnosti očistka, ima masa minimalni klinični pomen za farmakokinetiko anidulafungina.
Spol pripadnosti
Koncentracije anidulafungina v plazmi pri prostovoljcih in moških so bile podobne. V študijah, opravljenih pri bolnikih z več odmerki, je bil očistek zdravila nekoliko hitrejši (približno 22%) pri moških.
Upokojenci
Populacijska farmakokinetična analiza je pokazala, da se je mediani očistek nekoliko razlikoval med starejšo skupino (starost ≥ 65 let, mediana CL = 1,07 l / h) in starostno skupino (starost
Dirka
Farmakokinetika anidulafungina je bila pri kavkaških, črnih, azijskih in latinskoameriških osebah podobna.
HIV pozitivnost
Prilagoditev odmerka pri bolnikih s HIV ni potrebna, ne glede na sočasno protiretrovirusno zdravljenje.
Jetrna insuficienca
Anidulafungin se ne presnavlja v jetrih. Farmakokinetiko anidulafungina so proučevali pri osebah z jetrno okvaro stopnje A, B ali C. po Child-Pughovi koncentraciji.
Čeprav so pri bolnikih z jetrno okvaro stopnje C po Child-Pughu opazili rahlo zmanjšanje AUC, je bilo to zmanjšanje v okviru populacijskih ocen pri zdravih osebah.
Odpoved ledvic
Anidulafungin ima zanemarljiv ledvični očistek (normalno delovanje ledvic. Anidulafungin ni na dializi in ga je mogoče dajati ne glede na to, kdaj se izvaja dializa.
Pediatrični bolniki
Farmakokinetiko anidulafungina po vsaj 5 dnevnih odmerkih so proučevali pri 24 imunsko oslabljenih pediatričnih (starih 2-11 let) in mladostnikih (12-17 let) z nevtropenijo. The stacionarno stanje je bil dosežen prvi dan po polnilnem odmerku (dvakratni vzdrževalni odmerek) ter Cmax in AUCss pri stanje dinamičnega ravnovesja povečano na odmerek sorazmerno. Sistemska izpostavljenost po dajanju vzdrževalnega odmerka 0,75 mg in 1,5 mg / kg / dan / dan pri tej populaciji je bila primerljiva s tisto, ki so jo opazili pri odraslih po 50 oziroma 100 mg / dan. Ti bolniki so dobro prenašali oba režima odmerjanja.
05.3 Predklinični podatki o varnosti
V 3-mesečnih študijah so pri podganah in opicah, zdravljenih z odmerki 4-6-krat večjo od pričakovane klinične terapevtske izpostavljenosti, opazili dokaze o jetrni toksičnosti, vključno z zvišanjem encimov in morfološkimi spremembami. in vitro In in vivo z anidulafunginom ni zagotovil dokazov o genotoksičnem potencialu. Dolgoročne študije na živalih za oceno rakotvornega potenciala anidulafungina niso bile izvedene.
Dajanje anidulafungina pri podganah ni pokazalo vpliva na razmnoževanje, vključno s plodnostjo pri samcih in samicah.
Anidulafungin je pri podganah prešel placentno pregrado in je bil odkrit v plazmi ploda.
Študije o razvoju zarodka in ploda so bile izvedene z odmerki med 0,2 in 2-krat (podgane) in med 1 in 4-krat (zajci) predlaganim terapevtskim vzdrževalnim odmerkom 100 mg / dan. Anidulafungin pri podganah, testiranih pri največjem odmerku, ni povzročil nobene vrste razvojne toksičnosti, povezane z zdravili. Učinki na razvoj, opaženi pri kuncih (rahlo zmanjšana telesna masa), so se pojavili le pri največjem preizkušenem odmerku, odmerku, ki je povzročil tudi strupenost za mater.
Koncentracija anidulafungina v možganih je bila po enkratnem odmerku pri neokuženih odraslih in neonatalnih podganah nizka (razmerje možgani / plazma približno 0,2). Vendar so se koncentracije možganov pri neokuženih neonatalnih podganah po 5 dnevnih odmerkih povečale (razmerje možgani / plazma približno 0,7). V študijah z več odmerki pri kuncih z razširjeno kandidiazo in pri miših z okužbo CNS, ki jo povzroča Candida, anidulafungin je zmanjšal glivično obremenitev v možganih.
Podgane so zdravili s tremi odmerki anidulafungina in v eni uri anestezirali s kombinacijo ketamina in ksilazina. šele po anesteziji.
Pri živalih, zdravljenih z nižjim odmerkom v prisotnosti ali odsotnosti anestezije, in v skupini z vmesnimi odmerki v odsotnosti anestezije niso poročali o nobenih neželenih učinkih, z infuzijo povezanih reakcij ni bilo.
06.0 FARMACEVTSKE INFORMACIJE
06.1 Pomožne snovi
Fruktoza
Manitol
Polisorbat 80
Vinska kislina
Natrijev hidroksid (za uravnavanje pH)
Klorovodikova kislina (za uravnavanje pH)
06.2 Nezdružljivost
Tega zdravila ne smete mešati z drugimi zdravili, razen s tistimi, ki so omenjena v poglavju 6.6.
06.3 Obdobje veljavnosti
3 leta.
Dovoljeni so temperaturni izleti za 96 ur do 25 ° C, prašek pa lahko vrnete v hladilne pogoje.
Rekonstituirana raztopina:
Pripravljeno raztopino lahko shranite pri 25 ° C do 24 ur.
Kemijsko-fizikalna stabilnost pripravljene raztopine v uporabi je bila dokazana 24 ur pri 25 ° C.
Z mikrobiološkega stališča lahko ob upoštevanju optimalnih aseptičnih pogojev rekonstituirano raztopino uporabimo do 24 ur kasneje, če jo hranimo pri 25 ° C.
Raztopina za infundiranje:
Raztopino za infundiranje lahko shranimo pri 25 ° C 48 ur ali zamrznjeno vsaj 72 ur.
Kemijsko-fizikalna stabilnost infuzijske raztopine v uporabi je bila dokazana 48 ur pri 25 ° C.
Z mikrobiološkega vidika, ob upoštevanju optimalnih aseptičnih pogojev, lahko infuzijsko raztopino uporabimo 48 ur po pripravi, če jo hranimo pri 25 ° C.
06.4 Posebna navodila za shranjevanje
Shranjujte v hladilniku (2 ° C - 8 ° C).
Za pogoje shranjevanja po rekonstituciji in razredčitvi zdravila glejte poglavje 6.3.
06.5 Vrsta ovojnine in vsebina pakiranja
30 ml steklena viala tipa I z elastomernim zamaškom (butilna guma s prevleko iz inertnega polimera na površini v stiku z izdelkom in mazivom na zgornji površini za olajšanje izdelave) in aluminijastim tesnilom z zapiranjem na preklop.
Pakiranje z 1 vialo.
06.6 Navodila za uporabo in rokovanje
Ni posebnih navodil za odstranjevanje.
Zdravilo ECALTA je treba rekonstituirati samo z vodo za injekcije in nato razredčiti samo z raztopino natrijevega klorida 9 mg / ml (0,9%) za injiciranje z glukozo 50 mg / ml (5%) samo za infundiranje. Združljivost rekonstituiranega zdravila ECALTA z intravenskimi snovmi, dodatki ali zdravili, razen natrijevega klorida 9 mg / ml (0,9%) ali glukoze 50 mg / ml (5%), ni bila ugotovljena.
Rekonstitucija
Vsako vialo je treba v aseptičnih pogojih rekonstituirati s 30 ml vode za injekcije, da dobimo koncentracijo 3,33 mg / ml. Čas priprave lahko traja do 5 minut. Po naknadnem redčenju je treba raztopino zavreči, če se ugotovi prisotnost delcev ali razbarvanje.
Redčenje in infuzija
Vsebino rekonstituirane viale je treba pod aseptičnimi pogoji prenesti v intravensko vrečko (ali steklenico), ki vsebuje natrijev klorid za infundiranje 9 mg / ml (0,9%) ali glukozo za infundiranje 50 mg / ml 5%, da se doseže koncentracija anidulafungina 0,77 mg / ml. Spodnja tabela prikazuje količine, potrebne za vsak odmerek.
Zahteve za redčenje za dajanje zdravila ECALTA
Natrijev klorid za infundiranje 9 mg / ml (0,9%) ali glukoza za infundiranje 50 mg / ml (5%)
B Koncentracija raztopine za infundiranje je 0,77 mg / ml
Hitrost infundiranja ne sme presegati 1,1 mg / min (kar ustreza 1,4 ml / min, če ste pripravljeni in razredčeni po navodilih) (glejte poglavja 4.2, 4.4 in 4.8).
Kadar koli dovoljujeta raztopina in vsebnik, je treba parenteralna zdravila pred dajanjem vizualno pregledati glede prisotnosti delcev ali razbarvanja.Če se ugotovi prisotnost delcev ali razbarvanje, je treba raztopino zavreči.
Neuporabljena zdravila in odpadke, pridobljene iz tega zdravila, je treba odstraniti v skladu z lokalnimi predpisi
07.0 IMETNIK DOVOLJENJA ZA PROMET
Pfizer Limited
Ramsgate Road, sendvič
Kent, CT13 9NJ, Združeno kraljestvo.
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET
EU/1/07/416/002
038382026
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA
Datum prve odobritve: 20. september 2007
Datum zadnje obnove: 23. avgust 2012
10.0 DATUM REVIZIJE BESEDILA
26. avgust 2014