Zdravilne učinkovine: doksorubicin
Caelyx 2 mg / ml koncentrat za raztopino za infundiranje
Indikacije Zakaj se uporablja zdravilo Caelyx? Za kaj je to?
Caelyx je zdravilo proti raku.
Zdravilo Caelyx se uporablja za zdravljenje raka dojke pri bolnikih s tveganjem za težave s srcem. Zdravilo Caelyx se uporablja tudi za zdravljenje raka jajčnikov, ki se uporablja za ubijanje rakavih celic, zmanjšanje velikosti tumorja, upočasnitev rasti tumorja in podaljšanje njegovega preživetja.
Zdravilo Caelyx se uporablja tudi v kombinaciji z drugim zdravilom, bortezomibom, za zdravljenje multiplega mieloma, raka krvi, pri bolnikih, ki so prejeli vsaj eno predhodno zdravljenje.
Caelyx se uporablja tudi za izboljšanje Kaposijevega sarkoma, vključno s sploščenjem, bledo in celo zmanjšanjem velikosti tumorja. Drugi simptomi Kaposijevega sarkoma, na primer oteklina okoli tumorja, se lahko izboljšajo ali izginejo.
Caelyx vsebuje snov, ki je sposobna interakcije s celicami, da selektivno ubije rakave celice. Doksorubicinijev klorid, ki ga vsebuje Caelyx, je zaprt v zelo majhnih kroglicah, imenovanih pegilirani liposomi, ki olajšajo transport zdravila iz krvi v tumorsko tkivo in se tako izognejo njegovi razpršitvi v zdravem tkivu.
Kontraindikacije Kadar zdravila Caelyx ne smete uporabljati
Ne jemljite zdravila Caelyx
- če ste alergični na doksorubicinijev klorid ali katero koli sestavino tega zdravila (navedeno v poglavju 6).
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Caelyx
Povejte svojemu zdravniku o naslednjih pogojih:
- če se zdravite zaradi težav s srcem ali jetri;
- če imate sladkorno bolezen, saj zdravilo Caelyx vsebuje sladkor in bo zdravljenje s sladkorno boleznijo morda treba ustrezno prilagoditi;
- če imate Kaposijev sarkom in so vam odstranili vranico;
- če opazite razjede, razbarvanje ali nelagodje v ustih.
Otroci in mladostniki
Zdravila Caelyx se ne sme uporabljati pri otrocih in mladostnikih, ker ni znano, kako zdravilo vpliva nanje.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Caelyx
Povejte svojemu zdravniku ali farmacevtu
- če jemljete ali ste pred kratkim jemali katerokoli zdravilo, tudi če ste ga dobili brez recepta,
- o vseh zdravilih za raka, ki jih spremlja ali jih je spremljal v preteklosti, saj je "posebna pozornost potrebna pri tistih zdravilih, ki zmanjšujejo število belih krvnih celic, saj lahko to privede do" nadaljnjega zmanjšanja števila krvnih celic belci. Če niste prepričani o zdravljenju, ki ste ga prejeli, ali o boleznih, ki ste jih imeli, se posvetujte s svojim zdravnikom
Opozorila Pomembno je vedeti, da:
Nosečnost in dojenje
Preden vzamete katerokoli zdravilo, se posvetujte z zdravnikom ali farmacevtom.
Ker lahko učinkovina v zdravilu Caelyx, doksorubicinijev klorid, povzroči spremembe pri nerojenem otroku, je pomembno, da o tem obvestite svojega zdravnika, če mislite, da ste noseči. Ženske se morajo izogibati zanositvi, če se skupaj s partnerjem zdravijo z zdravilom Caelyx in še šest mesecev po prekinitvi zdravljenja.
Ker je doksorubicinijev klorid lahko škodljiv za dojenčke, morajo ženske pred začetkom zdravljenja z zdravilom Caelyx prenehati z dojenjem.
Vpliv na sposobnost upravljanja vozil in strojev
Ne vozite in ne upravljajte z orodji ali stroji, če ste po zdravljenju z zdravilom Caelyx utrujeni ali zaspani.
Odmerjanje, način in čas dajanja Kako uporabljati zdravilo Caelyx: odmerjanje
Caelyx je edinstvena formulacija. Ne smemo ga uporabljati zamenljivo z drugimi formulacijami doksorubicinijevega klorida.
Koliko se daje Caelyx
Če se zdravite zaradi raka na dojki ali jajčnikih, boste prejeli zdravilo Caelyx v odmerku 50 mg na vsak kvadratni meter vaše telesne površine (glede na vašo višino in telesno težo). Odmerek se ponavlja vsake 4 tedne, dokler bolezen ne napreduje in ne prenašate zdravljenja.
Če se zdravite zaradi multiplega mieloma in ste že prejeli vsaj eno predhodno terapijo, vam bodo zdravilo Caelyx dali v odmerku 30 mg na kvadratni meter vaše telesne površine (glede na vašo višino in telesno težo) z intravensko uporabo 1 uro, dano takoj po infuziji bortezomiba 4. dan 3-tedenskega režima zdravljenja z bortezomibom. Odmerek se bo ponavljal, dokler se ne odzovete zadovoljivo in ne prenašate zdravljenja.
Če se zdravite zaradi Kaposijevega sarkoma, boste zdravilo Caelyx prejeli v odmerku 20 mg na vsak kvadratni meter vaše telesne površine (glede na vašo višino in težo). Odmerek se ponovi vsaka 2 ali 3 tedne 2 ali 3 mesece; pozneje se bo ponovil, ko bo treba ohraniti izboljšanje njegovega stanja.
Kako se daje zdravilo Caelyx
Zdravnik vam bo dal zdravilo Caelyx kot kapljico (infuzijo) v veno. Odvisno od odmerka in indikacije bo to trajalo od 30 minut do več kot eno uro (tj. 90 minut).
Preveliko odmerjanje Kaj storiti, če ste vzeli preveč zdravila Caelyx
Akutno preveliko odmerjanje poslabša neželene učinke, kot so rane v ustih ali padec belih krvnih celic in krvnih ploščic. Zdravljenje bo obsegalo dajanje antibiotikov, transfuzijo trombocitov, uporabo dejavnikov, ki spodbujajo proizvodnjo belih krvnih celic, in simptomatsko zdravljenje ran v ustih.
Če imate dodatna vprašanja o uporabi zdravila Caelyx, se posvetujte z zdravnikom ali farmacevtom.
Neželeni učinki Kakšni so stranski učinki zdravila Caelyx
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih.
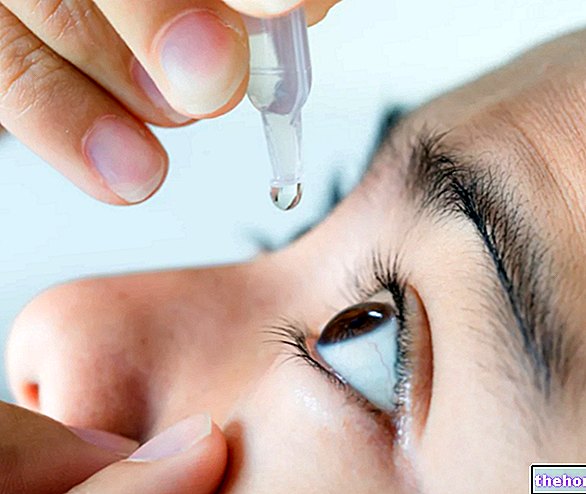
Med infundiranjem zdravila Caelyx se lahko pojavijo naslednje reakcije: zardevanje obraza, zadihanost, glavobol, mrzlica, bolečine v hrbtu, tesnost v prsih in / ali grlu, vneto grlo, visok ali nizek krvni tlak, povečan srčni utrip, otekanje obraz, zvišana telesna temperatura, omotica, slabost, prebavne motnje, srbenje, nenadna pordelost kože in potenje.V zelo redkih primerih so se pojavili napadi. Lahko se pojavi tudi pekoča bolečina ali oteklina na mestu injiciranja. Če vas med jemanjem zdravila Caelyx kapljanje neprijetno ali boleče, o tem nemudoma obvestite svojega zdravnika.
Takoj se obrnite na svojega zdravnika, če:
- na rokah in nogah se pojavi boleča rdečina,
- razvije boleč občutek na koži in / ali mehurčke na telesu ali v ustih,
- imate težave s srcem,
- ima rane v ustih,
- zvišana telesna temperatura ali drugi znaki okužbe,
- imate "nenadno zasoplost ali ostro bolečino v prsih, ki se lahko poslabša pri globokem dihanju ali kašljanju",
- imate otekanje, toploto ali občutljivost mehkih tkiv v nogah, včasih z bolečino, ki se poslabša, če stojite ali hodite.
Drugi stranski učinki
Med infuzijami se lahko pojavijo naslednji učinki:
Zelo pogosti (pojavijo se lahko pri več kot 1 od 10 bolnikov):
- pordelost, oteklina in rane na dlaneh in podplatih. Ti učinki so bili pogosto opaženi in so včasih resni. V hudih primerih lahko ti učinki motijo nekatere dnevne dejavnosti in lahko trajajo do 4 tedne ali dlje, preden se popolnoma razrešijo. Zdravnik lahko po lastni presoji odloži začetek in / ali zmanjša odmerek naslednjega zdravljenja (glejte Spodaj tehnike za preprečevanje in zdravljenje sindroma rok in stopal);
- bolečine ali rane v ustih ali grlu, slabost, bruhanje, driska, zaprtje, izguba apetita, izguba teže;
- zmanjšanje števila belih krvnih celic, kar lahko poveča možnost okužbe. Anemija (zmanjšanje števila rdečih krvnih celic) lahko povzroči utrujenost, znižanje krvnih ploščic pa poveča tveganje za krvavitev. V redkih primerih lahko nizko število belih krvnih celic povzroči resne okužbe. Zaradi možnih sprememb v krvne celice, potrebno je redno spremljanje krvi V klinični študiji pri bolnikih z AIDS-KS, ki so primerjali zdravilo Caelyx z drugim zdravljenjem (bleomicin / vinkristin), je bilo ugotovljeno, da obstaja večja možnost nekaterih okužb s Caelyxom. po izkušnjah pri bolnikih z AIDS-KS, ko je bilo zdravilo Caelyx primerjano s standardnim zdravljenjem napredovalega raka jajčnikov (topotekan), je bilo tveganje za okužbe v skupini bolnikov, zdravljenih s Caelyxom, bistveno manjše. Tveganje za nizko krvno sliko in okužbe je bilo podobno majhno v študijah raka dojke. Nekateri od teh učinkov so lahko povezani z boleznijo, ki ni Caelyx;
- splošen občutek utrujenosti, šibkosti, zatiča in igle ali bolečine v rokah in nogah;
- izguba las.
Pogosti (pojavijo se lahko pri največ 1 od 10 bolnikov):
- bolečine v trebuhu;
- ustni drozg (glivična okužba ust), rane v nosu, krvavitve iz nosu, herpes in vnetje jezika;
- vrednosti jetrnih testov se lahko med zdravljenjem z zdravilom Caelyx povečajo ali zmanjšajo;
- zaspanost, omotica, omedlevica, bolečine v kosteh, bolečine v prsih, nenormalna mišična napetost, mišične bolečine, krči ali otekanje spodnjih okončin, splošno otekanje, vnetje mrežnice (očesna membrana, stimulirana s svetlobo), povečano solzenje, zamegljen vid , občutek zatičev in igel ali bolečine v rokah in nogah;
- vnetje lasnih mešičkov, luščenje kože, vnetje ali izpuščaj, nenormalna pigmentacija (razbarvanje) težav s kožo in nohti;
- težave s srcem, npr. nepravilen srčni utrip, razširjene krvne žile;
- zvišana telesna temperatura, zvišana telesna temperatura ali drugi znaki okužbe, ki so lahko povezani z boleznijo;
- težave z dihanjem, to je težave pri dihanju ali kašljanju, ki so lahko povezane z okužbami, ki so posledica bolezni;
- premalo vode v telesu (dehidracija), huda izguba teže in izguba mišične mase, nizke ravni kalcija, magnezija, kalija ali natrija v krvi, visoke ravni kalija v krvi;
- vnetje požiralnika (ezofagitis), vnetje želodčne sluznice, težave pri požiranju, suha usta, napenjanje, vnetje dlesni (gingivitis), spremembe v občutku okusa;
- vnetje vagine;
- bolečine pri uriniranju;
- če ste med zdravljenjem s sevanjem že imeli kožne reakcije, tj. bolečino, pordelost in suhost kože, se lahko te med zdravljenjem s Caelyxom še vedno pojavijo;
- bolečine v sklepih, zmanjšan ali nenormalen občutek pri stimulaciji, lahko pride do vnetja roženice, rdečih oči, rdečega skrotuma pri kombinaciji zdravila Caelyx in bortezomiba. Ko se zdravilo Caelyx uporablja samostojno, so nekateri od teh učinkov manj verjetni, nekateri pa se ne pojavijo pri vse.
Občasni (pojavijo se pri največ 1 od 100 bolnikov)
- zmedenost;
- vnetje žil in nastanek krvnih strdkov v venah, ki lahko blokirajo pretok krvi v pljuča in povzročijo težave pri dihanju, bolečine v prsih in palpitacije.
Zelo redki (pojavijo se pri največ 1 od 10.000 bolnikov)
- hude kožne reakcije, kot so razširjeno luščenje kože, mehurji in erozija (razjede) sluznice (Stevens-Johnsonov sindrom / toksična epidermalna nekroliza);
- Rak ust se lahko pojavi, če zdravilo Caelyx jemljete dlje časa (več kot eno leto).
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom ali medicinsko sestro.To vključuje vse možne neželene učinke, ki niso navedeni v tem navodilu. zagotovite več informacij o varnosti tega zdravila.
Tehnike za preprečevanje in zdravljenje sindroma rok in stopal vključujejo:
- če je le mogoče, potopite roke in / ali noge v umivalnik s hladno vodo (npr. med gledanjem televizije, branjem ali poslušanjem radia);
- roke in noge naj bodo nepokrite (brez rokavic, nogavic itd.)
- ostati na hladnem;
- v vročih obdobjih si privoščite hladne kopeli;
- izogibajte se intenzivni vadbi, ki lahko povzroči poškodbe stopal (npr. tek);
- izogibajte se izpostavljanju kože zelo vroči vodi (npr. hidromasaža, savna);
- izogibajte se tesnim čevljem ali čevljem z visokimi petami.
Piridoksin (vitamin B6):
- vitamin B6 je mogoče kupiti brez recepta;
- jemljite 50-150 mg na dan, pri prvih znakih pordelosti ali mravljinčenja.
Potek in zadržanje
Zdravilo Caelyx shranjujte nedosegljivo otrokom!
Shranjujte v hladilniku (2 ° C - 8 ° C). Ne zamrzujte.
Po redčenju:
- Kemična in fizikalna stabilnost med uporabo je bila dokazana 24 ur pri temperaturah med 2 ° C in 8 ° C.
- Z mikrobiološkega vidika je treba izdelek uporabiti takoj. Če se ne uporabi takoj, je za čas shranjevanja in metode razredčene raztopine pred uporabo odgovoren uporabnik in ne sme presegati 24 ur, če je shranjena pri temperaturah med 2 ° C in 8 ° C. Delno uporabljene viale je treba izbrisati.
Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na nalepki in škatli.
Tega zdravila ne uporabljajte, če opazite oborino ali druge vrste delcev.
Ne mečite nobenih zdravil v odpadne vode ali med gospodinjske odpadke. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Tako boste zaščitili okolje.
Druge informacije
Kaj vsebuje zdravilo Caelyx
- Zdravilna učinkovina je doksorubicinijev klorid. En ml zdravila Caelyx vsebuje 2 mg doksorubicinijevega klorida v pegilirani liposomski formulaciji.
- Druge sestavine so?-(2- [1,2-distearoil-sn-glicerofosfoksi] etilkarbamoil)-omega-metoksi poli (oksietilen) -40 natrijeva sol (MPEG-DSPE), popolnoma hidrogeniran sojin fosfatidilholin (HSPC), holesterol, amonijev sulfat, saharoza, histidin, voda za injekcije, klorovodikova kislina in natrijev hidroksid.
Caelyx 2 mg / ml koncentrat za raztopino za infundiranje: viale, ki lahko dajo volumen 10 ml (20 mg) ali 25 ml (50 mg).
Izgled zdravila Caelyx in vsebina pakiranja
Raztopina za infundiranje je sterilna, prosojna in rdeča. Caelyx je na voljo v steklenih ampulah v posameznih pakiranjih ali v 10 vialah.
Na trgu ni vseh navedenih pakiranj.
Naslednje informacije so namenjene samo zdravnikom in zdravstvenim delavcem:
Z raztopino Caelyx je treba ravnati previdno. Če pride Caelyx v stik s kožo ali sluznico, jih je treba nemudoma temeljito umiti z milom. Z zdravilom Caelyx je treba ravnati in jih odstraniti v skladu s previdnostnimi ukrepi, navedenimi pri drugih zdravilih proti raku.
Določite odmerek zdravila Caelyx, ki ga boste uporabili (odvisno od priporočenega odmerka in bolnikove telesne površine). S sterilno brizgo izvlecite pravilen volumen zdravila Caelyx. Delovati je treba v strogo aseptičnih pogojih, saj Caelyx ne vsebuje konzervansov ali bakteriostatikov. Pred dajanjem je treba pravilen odmerek zdravila Caelyx razredčiti v 5% raztopini glukoze (50 mg / ml) za intravensko infuzijo. Za odmerke <90 mg razredčite Caelyx v 250 ml in za odmerke? 90 mg razredčenega Caelyxa v 500 ml.
Za zmanjšanje tveganja infuzijskih reakcij je treba začetni odmerek dajati s hitrostjo, ki ne presega 1 mg / min.Če infuzijske reakcije ne opazimo, lahko naslednje infuzije zdravila Caelyx dajemo v obdobju 60 minut.
V programu kliničnega preskušanja raka dojke je bila infuzija dovoljena pri tistih bolnikih, pri katerih je prišlo do reakcije po dajanju, kot je naslednja: 5% celotnega odmerka so v prvih 15 minutah dajali počasi. hitrost se je v naslednjih 15 minutah podvojila.Če je bolnik toleriral, je bila infuzija končana v naslednji uri, kar je trajalo skupno 90 minut injiciranja.
Če ima bolnik zgodnje simptome ali znake infuzijske reakcije, infuzijo takoj prekinite, dajte ustrezne premedikacije (antihistaminike in / ali kratkodelujoče kortikosteroide) in infuzijo nadaljujte počasneje.
Uporaba razredčil, ki niso 5% raztopina glukoze (50 mg / ml) za intravensko infuzijo ali prisotnost katerega koli bakteriostatičnega sredstva, kot je benzil alkohol, lahko povzroči obarjanje Caelyxa.
Priporočljivo je, da infuzijsko linijo, ki vsebuje Caelyx, povežete s stranskim dovodom intravenske infuzije 5% glukoze (50 mg / ml). Infuzijo lahko dovajate skozi periferno veno. Ne uporabljajte z vgrajenimi filtri.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA
CAELYX 2 mg / ml koncentrat za raztopino za infuzijo
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA
En ml zdravila Caelyx vsebuje 2 mg doksorubicinijevega klorida v pegilirani liposomski formulaciji.
Caelyx je sestavljen iz liposomske formulacije, v kateri je doksorubicinijev klorid inkapsuliran v liposome, na površino katerih je vezan metoksi polietilen glikol (MPEG). Ta proces, znan kot pegilacija, ščiti liposome pred prepoznavanjem fagocitnega mononuklearnega sistema (MPS), kar povečuje njihov čas kroženja v krvi.
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA
Koncentrat za raztopino za infundiranje
Suspenzija je sterilna, prosojna in rdeča.
04.0 KLINIČNE INFORMACIJE
04.1 Terapevtske indikacije
Zdravilo Caelyx je indicirano:
- Kot monoterapija pri bolnikih z metastatskim rakom dojke, pri katerih obstaja povečano tveganje za srce.
-Za zdravljenje napredovalega raka jajčnikov pri ženskah, ki niso uspele na prvi liniji kemoterapije na osnovi platine.
- V kombinaciji z bortezomibom za zdravljenje progresivnega multipla mieloma pri bolnikih, ki so bili predhodno vsaj enkrat zdravljeni in so že bili ali ne morejo presaditi kostnega mozga.
-Za zdravljenje Kaposijevega sarkoma, povezanega z aidsom (KS-AIDS), pri bolnikih z nizkim številom CD4 (limfociti CD4 3) in razpršeno sluznico ali visceralno boleznijo.
Zdravilo Caelyx se lahko uporablja kot prva ali druga linija sistemske kemoterapije pri bolnikih z AIDS-KS z napredovalo boleznijo ali pri bolnikih, ki ne prenašajo predhodne sistemske kombinirane kemoterapije z vsaj dvema od naslednjih snovi: vinka alkaloidom, bleomicinom in standardnim doksorubicinom ( ali "drug antraciklin").
04.2 Odmerjanje in način uporabe
Zdravilo Caelyx je treba dajati le pod nadzorom onkologa, ki je specializiran za dajanje citotoksičnih zdravil.
Caelyx ima edinstvene farmakokinetične lastnosti; zato ga ne smemo uporabljati zamenljivo z drugimi formulacijami doksorubicinijevega klorida.
Rak dojke / rak jajčnikov :
Zdravilo Caelyx je treba dajati intravensko v odmerku 50 mg / m2 enkrat na 4 tedne, dokler bolezen ne napreduje in bolnik ne prenaša zdravljenja.
Multipli mielom : Zdravilo Caelyx se daje v odmerku 30 mg / m2 4. dan 3-tedenskega režima bortezomiba v obliki 1-urne intravenske infuzije takoj po infuziji bortezomiba.Režim bortezomiba je sestavljen iz odmerka 1,3 mg / m2 na dan 1, 4, 8 in 11 vsake 3 tedne. Terapijo je treba ponavljati, dokler ima bolnik zadovoljiv odziv in je sposoben prenašati zdravljenje. Odmerek obeh zdravil na 4. dan se lahko po medicinski potrebi odloži do 48 ur .Doze bortezomiba je treba ločiti vsaj 72 ur.
Za intravenske odmerke.
Za odmerke ≥ 90 mg: razredčite Caelyx v 500 ml 5% raztopine glukoze (50 mg / ml) za intravensko infuzijo.
Da bi zmanjšali tveganje za reakcije, povezane z infuzijo, je treba začetni odmerek dajati s hitrostjo, ki ne presega 1 mg / minuto.Če reakcij ni opaziti, lahko naslednje infuzije zdravila Caelyx dajemo v 60 minutah.
Pri tistih bolnikih, ki so imeli po dajanju reakcijo, je bila dovoljena sprememba infuzije, na primer naslednja:
5% celotnega odmerka je treba v prvih 15 minutah dajati počasi. Če bolnik prenaša brez reakcije, se lahko hitrost infundiranja v naslednjih 15 minutah podvoji. Če prenašate, lahko infuzijo dokončate v naslednji uri za skupni čas injiciranja 90 minut.
Kaposijev sarkom, povezan z aidsom :
Zdravilo Caelyx se daje intravensko v odmerkih 20 mg / m2 vsaka dva do tri tedne. Izogibajte se intervalom, manjšim od 10 dni, saj kopičenja proizvoda in povečanja toksičnosti ni mogoče izključiti. Za doseganje terapevtskega odziva je priporočljivo, da se bolniki zdravijo dva do tri mesece. Po potrebi nadaljujte z zdravljenjem, da ohranite terapevtski odziv.
Odmerek zdravila Caelyx razredčimo v 250 ml 5% raztopine glukoze (50 mg / ml) za intravensko infuzijo in jo dajemo z intravensko infuzijo v 30 minutah.
Za vse bolnike :
Če se pri bolniku pojavijo prvi znaki ali simptomi infuzijske reakcije (glejte poglavji 4.4 in 4.8), infuzijo takoj prekinite, dajte ustrezne premedikacije (antihistaminike in / ali kratkodelujoče kortikosteroide) in nadaljujte z infuzijo pozneje. Počasneje.
Ne dajajte zdravila Caelyx kot bolus ali nerazredčeno raztopino. Priporočljivo je, da infuzijsko cev, ki vsebuje Caelyx, povežete s stranskim dovodom intravenske infuzije 5% glukoze (50 mg / ml), da dodatno raztopite raztopino in zmanjšate tveganje za trombozo in ekstravazacijo. Infuzijo lahko dajemo skozi periferno veno. Ne uporabljajte je z linijskimi filtri. Caelyxa ne smete dajati intramuskularno ali podkožno (glejte poglavje 6.6).
Za obvladovanje neželenih dogodkov, kot so palmarno-plantarna eritrodisestezija (OZO), stomatitis ali hematološka toksičnost, se lahko odmerek zmanjša ali preloži. Smernice za prilagoditev odmerka zdravila Caelyx po teh neželenih dogodkih so navedene v spodnjih tabelah.Klasifikacija strupenosti v teh tabelah temelji na skupnih merilih toksičnosti Nacionalnega inštituta za raka (NCI-CTC).
Tabele za osebno zaščitno opremo (tabela 1) in stomatitis (preglednica 2) podajajo shemo za prilagajanje odmerka med kliničnimi preskušanji pri zdravljenju raka dojke ali jajčnikov (sprememba priporočenega 4-tedenskega zdravljenja): če se te toksičnosti pojavijo pri bolnikih s KS-AIDS-om se lahko priporočeni potek zdravljenja 2-3 tedne podobno spremeni.
Tabela s hematološko toksičnostjo (preglednica 3) vsebuje shemo za spreminjanje odmerka med kliničnimi študijami, opravljenimi samo pri bolnikih z rakom dojke ali jajčnikov. Za prilagoditev odmerka pri bolnikih z AIDS-KS glejte poglavje 4.8.
Smernice za prilagoditev odmerka Caelyxa
Pri bolnikih z multiplim mielomom, zdravljenih z zdravilom Caelyx v kombinaciji z bortezomibom, pri katerih se razvije osebna zaščitna oprema ali stomatitis, je treba odmerek zdravila Caelyx prilagoditi, kot je opisano v preglednicah 1 in 2 zgoraj. V spodnji preglednici 4 je prikazana shema za druge prilagoditve odmerka med kliničnim preskušanjem pri bolnikih z multiplim mielomom, ki so prejemali zdravilo Caelyx in bortezomib v kombinirani terapiji. Za več informacij o odmerjanju in prilagoditvi odmerka bortezomiba glejte tudi Povzetek glavnih značilnosti bortezomiba (SmPC).
* za več informacij o odmerjanju bortezomiba in prilagoditvah odmerka glejte povzetek glavnih značilnosti zdravila bortezomib
Bolniki z jetrno insuficienco : farmakokinetika zdravila Caelyx, ugotovljena pri majhnem številu bolnikov s povišanim nivojem skupnega bilirubina, se ne razlikuje od farmakokinetike pri normalnem skupnem bilirubinu; dokler ni na voljo več informacij, je treba odmerek zdravila Caelyx pri bolnikih z jetrno insuficienco zmanjšati na podlagi izkušenj iz kliničnih preskušanj pri raku dojk in jajčnikov, in sicer: na začetku zdravljenja, če je bilirubin med 1,2 in 3,0 mg / dl se prvi odmerek zmanjša za 25%. Če je bilirubin> 3,0 mg / dl, se prvi odmerek zmanjša za 50%. Če bolnik prenaša prvi odmerek brez povečanja serumskega bilirubina ali jetrnih encimov, se lahko odmerek drugega cikla poveča na naslednjo raven, to je, če se prvi odmerek zmanjša za 25%, se polni odmerek poveča na drugi cikel; če se je prvi odmerek zmanjšal za 50%, v drugem ciklu povečajte na 75% celotnega odmerka. Če se tolerira, se lahko odmerek v naslednjih ciklih poveča na polni odmerek. Zdravilo Caelyx lahko dajemo bolnikom z jetrnimi metastazami in sočasnim povečanjem bilirubina in jetrnih encimov do 4 -kratne zgornje meje normalnega območja. fosfataze in bilirubina.
Bolniki z ledvično insuficienco : Ker se doksorubicin presnavlja v jetrih in se izloča z žolčem, prilagajanje odmerka ni potrebno. Populacijski farmakokinetični podatki (v preskušenem območju očistka kreatinina 30-156 ml / min) kažejo, da ledvična funkcija ne vpliva na izločanje Caelyxa. Farmakokinetičnih podatkov pri bolnikih z očistkom kreatinina ni več.
Splenektomirani bolniki s KS-AIDS-om : Ker ni izkušenj z uporabo zdravila Caelyx pri bolnikih na splenektomiji, njegova uporaba ni priporočljiva.
Pediatrični bolniki : Izkušnje pri otrocih so omejene. Zdravilo Caelyx ni priporočljivo pri bolnikih, mlajših od 18 let.
Starejši bolniki : Populacijska analiza kaže, da starost v testiranem razponu (21-75 let) ne spremeni bistveno farmakokinetike zdravila Caelyx.
04.3 Kontraindikacije
• Preobčutljivost za zdravilno učinkovino ali katero koli pomožno snov.
Zdravila Caelyx se ne sme uporabljati za zdravljenje AIDS-KS, ki ga je mogoče učinkovito zdraviti z lokalno terapijo ali s sistemskim alfa-interferonom.
04.4 Posebna opozorila in ustrezni previdnostni ukrepi za uporabo
Srčna toksičnost : Priporočljivo je, da se vsem bolnikom, zdravljenim s Caelyxom, redno izvaja elektrokardiogram (EKG). Prehodne spremembe v vzorcu EKG, kot so sploščenje vala T, podniveliranje segmenta ST in benigne aritmije, se ne štejejo za zavezujoče signale za prekinitev zdravljenja s Caelyxom, vendar se zmanjšanje kompleksa QRS šteje za najbolj indikativni znak srčnega do te spremembe pride v poštev odločilni test za toksičnost miokarda za antraciklin, to je endomiokardialna biopsija.
Bolj specifične metode elektrokardiograma za vrednotenje in nadzor srčne funkcije so merjenje iztisne frakcije levega prekata z ehokardiografijo ali po možnosti z arteriografijo z več vrati (MUGA). Te metode je treba uporabljati rutinsko pred do začetka zdravljenja z zdravilom Caelyx in ga je treba med zdravljenjem občasno ponavljati. Ocena delovanja levega prekata je bistvena pred kakršno koli dodatno uporabo zdravila Caelyx, ki presega dovoljeni kumulativni odmerek antraciklina v življenjski dobi 450 mg / m2.
Ocenjevalne teste in zgoraj opisane metode v zvezi s spremljanjem srca med zdravljenjem z antraciklini je treba uporabiti v naslednjem vrstnem redu: spremljanje EKG -ja, merjenje iztisne frakcije levega prekata, endomiokardialna biopsija. terapijo je treba skrbno pretehtati glede na tveganje za poškodbe miokarda.
Bolnike s srčnimi boleznimi, ki potrebujejo zdravljenje z zdravilom Caelyx, zdravite le, če korist odtehta tveganje.
Pri bolnikih z okvarjenim delovanjem srca, ki se zdravijo z zdravilom Caelyx, je potrebna previdnost.
Kadar obstaja sum na kardiomiopatijo, to je, ko se je iztisni delež levega prekata bistveno zmanjšal v primerjavi z vrednostmi pred zdravljenjem in / ali je iztisni delež levega prekata nižji od ustrezne vrednosti s prognostičnega vidika (npr.
Kongestivno srčno popuščanje zaradi kardiomiopatije se lahko pojavi nenadoma, tudi nekaj tednov po prekinitvi zdravljenja, ne da bi mu sledile spremembe na elektrokardiogramu.
Pri bolnikih, zdravljenih z drugimi antraciklini, je potrebna previdnost. Celotni odmerek doksorubicinijevega klorida mora upoštevati tudi vse predhodne (ali sočasne) terapije s kardiotoksičnimi spojinami, kot so drugi antraciklini / antrakinoni ali npr. 5-fluorouracil. Srčna toksičnost se lahko pojavi tudi pri kumulativnih odmerkih antraciklinov pod 450 mg / m2 pri bolnikih s predhodnim obsevanjem mediastinuma ali pri bolnikih, ki se sočasno zdravijo s ciklofosfamidom.
Na ravni srca je varnostni profil priporočenega odmerjanja pri raku dojk in jajčnikov (50 mg / m2) primerljiv s tistim pri 20 mg / m2 pri bolnikih z AIDS-KS (glejte poglavje 4.8).
Mielosupresija : Mnogi bolniki, zdravljeni z zdravilom Caelyx, imajo mielosupresijo zaradi različnih dejavnikov, kot so že obstoječa okužba s HIV ali številne sočasne ali prejšnje terapije ali tumorji, ki vključujejo kostni mozeg. V ključni študiji pri bolnikih z rakom jajčnikov, zdravljenih s 50 mg / m2, je bila mielosupresija na splošno blaga do zmerna, reverzibilna in ni bila povezana z epizodami nevtropenične okužbe ali sepse. Poleg tega je bila v kontroliranem kliničnem preskušanju zdravila Caelyx v primerjavi s topotekanom incidenca sepse, povezane z zdravljenjem, v skupini z rakom jajčnikov, zdravljenih s Caelyxom, bistveno manjša kot v skupini, zdravljeni s topotekanom. Podobno nizko pojavnost mielosupresije so opazili pri bolnikih. z metastatskim rakom dojke, ki se zdravi s Caelyxom v prvem kliničnem preskušanju. V nasprotju z izkušnjami pri bolnikih z rakom dojk ali jajčnikov se zdi, da je mielosupresija pri bolnikih z AIDS-KS omejevalni odmerek (glejte poglavje 4.8) zaradi možnosti mieloablacije je treba med zdravljenjem z zdravilom Caelyx in vsaj pred vsakim odmerkom zdravila Caelyx pogosto izvajati redne krvne preiskave.
Huda in vztrajna mielosupresija lahko povzroči superinfekcijo ali krvavitev.
V kontroliranih kliničnih preskušanjih pri bolnikih z AIDS-KS v primerjavi z režimom bleomicina / vinkristina so bile oportunistične okužbe med zdravljenjem s Caelyxom očitno pogostejše. Bolniki in zdravniki se morajo zavedati te povečane pojavnosti in ustrezno ukrepati.
Tako kot pri drugih antineoplastičnih zdravilih, ki poškodujejo DNA, so pri bolnikih, ki so prejemali kombinirano zdravljenje z doksorubicinom, poročali o sekundarnih akutnih mieloičnih levkemijah in mielodisplazijah. Zato mora biti vsak bolnik, zdravljen z doksorubicinom, pod hematološkim nadzorom.
Zaradi razlike v farmakokinetičnem profilu in režimu odmerjanja se zdravila Caelyx ne sme uporabljati sočasno z drugimi formulacijami doksorubicinijevega klorida.
Reakcije, povezane z infuzijo : V nekaj minutah po začetku infuzije zdravila Caelyx se lahko pojavijo hude in včasih smrtno nevarne infuzijske reakcije, za katere so značilne alergijske ali anafilaktoidne reakcije, katerih simptomi vključujejo astmo, zardevanje, srbenje izpuščaja, bolečine v prsih, zvišano telesno temperaturo, tahikardijo, srbenje, znojenje težko dihanje, edem obraza, mrzlica, bolečine v hrbtu, tesnost v prsih in grlu ter / ali hipotenzija Zelo redko so opazili krče kot reakcijo pri infuziji (glejte poglavje 4.8). Običajno začasna prekinitev infuzije odpravi te simptome brez nadaljnjega terapevtskega posega, vendar morajo biti za takojšnjo uporabo na voljo zdravila za zdravljenje teh simptomov (na primer antihistaminiki, kortikosteroidi, epinefrin in antikonvulzivi) ter oprema za nujne primere. pri bolnikih se lahko zdravljenje nadaljuje po odpravi vseh simptomov brez ponovitve .. Reakcije na infuzijo se po prvem poteku zdravljenja redko ponovijo. Za zmanjšanje tveganja infuzijskih reakcij je treba začetni odmerek dati s hitrostjo infundiranja, ki ne presega 1 mg / minuto (glejte poglavje 4.2).
Bolniki s sladkorno boleznijo : Upoštevati je treba, da vsaka viala zdravila Caelyx vsebuje saharozo in se daje kot 5% raztopina glukoze (50 mg / ml) za intravensko infuzijo.
Za pogoste neželene učinke, ki zahtevajo spremembo odmerka ali prekinitev, glejte poglavje 4.8.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij
Uradnih študij medsebojnega delovanja med drugimi zdravili in zdravilom Caelyx niso izvedli, čeprav so bile pri bolnikih z ginekološkim rakom opravljene kombinacijske študije faze II s konvencionalnimi kemoterapevtiki. Pri sočasni uporabi zdravil, za katera je znano, da medsebojno delujejo s standardnim doksorubicinijevim kloridom, je potrebna previdnost. Caelyx lahko tako kot drugi pripravki doksorubicinijevega klorida poveča toksičnost drugih zdravil proti raku. V kliničnih preskušanjih pri bolnikih s solidnimi tumorji (vključno z rakom dojk in jajčnikov) sočasno s ciklofosfamidom ali taksani niso našli novih kumulativnih toksičnih učinkov.Pri bolnikih z aidsom so po uporabi standardnega doksorubicinijevega klorida opazili primere poslabšanja hemoragičnega cistitisa, ki ga je povzročil ciklofosfamid, in povečane hepatotoksičnosti 6-merkaptopurina. Previdnost je potrebna tudi, kadar je potrebna sočasna uporaba drugih citotoksičnih zdravil, zlasti mielotoksičnih.
04.6 Nosečnost in dojenje
Nosečnost : Doksorubicinijev klorid naj bi povzročil resne okvare pri rojstvu, če ga dajemo med nosečnostjo. Zato se zdravila Caelyx med nosečnostjo ne sme uporabljati, razen če je to nujno potrebno.
Ženskam v rodni dobi je treba svetovati, naj se izogibajo nosečnosti, ne glede na to, ali se s partnerjem zdravijo z zdravilom Caelyx ali v šestih mesecih po koncu zdravljenja z zdravilom Caelyx (glejte poglavje 5.3).
Čas hranjenja : Ni znano, ali se Caelyx izloča v materino mleko. Ker se številna zdravila, vključno z antraciklini, izločajo v materino mleko in zaradi možnosti resnih neželenih učinkov na otroka, mora mati pred začetkom zdravljenja z zdravilom Caelyx prenehati z dojenjem. Zdravstveni strokovnjaki svetujejo ženskam, okuženim s HIV, da pod nobenim pogojem ne dojijo svojih otrok, da preprečijo prenos virusa HIV.
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji
Caelyx nima vpliva ali ima zanemarljiv vpliv na sposobnost vožnje in upravljanja s stroji. Dosedanje klinične študije pa kažejo, da zaspanost in zaspanost nista pogosto povezani (
04.8 Neželeni učinki
Najpogostejši neželeni učinek, o katerem so poročali v kliničnih preskušanjih raka dojke / jajčnikov (50 mg / m2 vsake 4 tedne), je bila palmarno -plantarna eritrodisestezija (PPE) .Splošna poročana pogostnost uporabe osebne zaščitne opreme je bila 44,0% - 46,1%. Ti učinki so bili večinoma blagi, v 17% - 19,5% pa so poročali o hudih primerih (stopnja III). Poročali so o življenjsko nevarnih primerih (IV. Stopnja), pri čemer so bile roke in noge pri nizkih temperaturah, pri čemer so bile v hladni vodi (namakanje, kopanje ali plavanje), izogibanje prekomernim virom toplote / vroče vode in nobenih zožitev (brez nogavic, rokavic ali tesni čevlji) Zdi se, da je OZO v glavnem povezana z režimom odmerjanja in ga je mogoče zmanjšati s povečanjem intervala med odmerki na 1-2 tedna (glejte poglavje 4.2). Vendar je lahko pri nekaterih bolnikih ta reakcija huda in izčrpavajoča ter zahteva prekinitev zdravljenja.Stomatitis / mukozitis in slabost so pogosto poročali tudi pri osebah, zdravljenih zaradi raka dojke / jajčnikov, pri bolnikih z AIDS-KS (20 mg / m2) vsaka 2 tedna) je bil najpogostejši neželeni učinek mielosupresija (predvsem levkopenija) (glejte KS-AIDS). O primerih osebne zaščitne opreme so poročali pri 16% bolnikov z multiplim mielomom, zdravljenih z zdravilom Caelyx v kombinaciji z bortezomibom. O stopnji 3 so poročali pri 5% Bolniki niso poročali o primerih osebne zaščitne opreme 4. stopnje. Najpogosteje poročani neželeni učinki (povezani ali zaradi terapije) pri kombiniranem zdravljenju (Caelyx + bortezomib) so bili (40%), driska (35%), nevtropenija (33%). , trombocitopenija (29%), bruhanje (28%), utrujenost (27%) in zaprtje (22%).
Rak na dojki : V klinični študiji faze III (I97-328) je bilo 509 bolnic z napredovalim rakom dojke, ki še niso prejemale kemoterapije zaradi metastatske bolezni, zdravili s Caelyxom (n = 254) v odmerku 50 mg / m2 vsake 4 tedne ali z doksorubicinom (n = 255) v odmerku 60 mg / m2 vsake 3 tedne. Pri doksorubicinu so pogosteje kot pri zdravilu Caelyx poročali o naslednjih pogostih neželenih učinkih: slabost (53% proti 37%; stopnja III / IV stopnje 5% proti 3%), bruhanje (31% proti 19%; stopnja III / IV 4 % proti manj kot 1%), različne manifestacije alopecije (66% proti 20%), izrazite alopecije (54% proti 7%) in nevtropenije (10% proti 4%; stopnja III / IV 8% proti 2%).
Pri zdravilu Caelyx so pogosteje kot pri doksorubicinu poročali o mukozitisu (23% proti 13%; stopnja III / IV 4% proti 2%) in stomatitisu (22% proti 15%; stopnja III / IV stopnje 5% proti 2%) . Povprečno trajanje najpogostejših resnih dogodkov (stopnja III / IV) za obe skupini je bilo 30 dni ali manj. Za celoten seznam neželenih učinkov, o katerih so poročali pri bolnikih, zdravljenih z zdravilom Caelyx, glejte tabelo 5.
Incidenca smrtno nevarnih (IV. Stopnja) hematoloških učinkov je bila
Klinično pomembne laboratorijske nepravilnosti (stopnje III in IV) so bile v tej skupini le redke, z zvišano koncentracijo celotnega bilirubina, AST in ALT pa v 2,4%, 1,6% in
* palmarno-plantarna eritrodisestezija (sindrom roke in noge).
Rak jajčnikov : 512 bolnikov z rakom jajčnikov (podskupina 876 bolnikov s solidnimi tumorji) je bilo v kliničnih preskušanjih zdravljenih z zdravilom Caelyx v odmerku 50 mg / m2. Za neželene učinke, o katerih so poročali pri bolnikih, zdravljenih s Caelyxom, glejte preglednico 6.
* palmarno-plantarna eritrodisestezija (sindrom roke-stopala).
Mielosupresija je bila večinoma blaga do zmerna in obvladljiva. Sepse, povezane z levkopenijo, niso opazili pogosto (
V subpopulaciji 410 bolnikov z rakom jajčnikov so klinično pomembne spremembe laboratorijskih parametrov med kliničnimi preskušanji z zdravilom Caelyx vključevale zvišanje skupnega bilirubina (običajno pri bolnikih z jetrnimi metastazami) (5%) in serumske vrednosti kreatinina (5%). Manj pogosto so poročali o zvišanju ravni AST (
Bolniki s trdnimi tumorji: V večji kohortni študiji 929 bolnikov s solidnimi tumorji (vključno z rakom dojk in jajčnikov), zdravljenih večinoma v odmerku 50 mg / m2 vsake 4 tedne, sta bila varnostni profil in pojavnost neželenih učinkov primerljiva s tistimi pri zdravljenih bolnikih v pilotnih preskušanjih raka dojke in jajčnikov.
Multipli mielom: V študiji faze III je bilo od 646 bolnikov z multiplim mielomom, ki so predhodno prejemali vsaj eno zdravljenje, 318 zdravljenih s Caelyxom 30 mg / m2, danim v obliki 1 urne intravenske infuzije na 4. dan zdravljenja z bortezomibom. Bortezomib so dajali v odmerku 1,3 mg / m2 1., 4., 8. in 11. dan vsake tri tedne v kombinaciji s Caelyxom ali kot monoterapijo. Za neželene učinke, o katerih so poročali pri ≥ 5% bolnikov, zdravljenih s kombiniranim zdravljenjem z zdravilom Caelyx in bortezomibom, glejte preglednico 7.
Nevtropenija, trombocitopenija in anemija so bili najpogosteje opisani hematološki neželeni učinki s kombinacijo samo Caelyxa in bortezomiba ter samo bortezomiba. Incidenca nevtropenije 3. in 4. stopnje je bila v skupini s kombiniranim zdravljenjem višja kot v skupini s kombiniranim zdravljenjem. pri monoterapiji (28% proti 14%). Incidenca trombocitopenije 3. in 4. stopnje je bila pri kombiniranem zdravljenju večja kot pri monoterapiji (22% v primerjavi s 14%). Incidenca anemije je bila v obeh skupinah primerljiva (7% v primerjavi s 5%).
V kombinirani skupini (16%) so poročali o primerih stomatitisa pogosteje kot v skupini z monoterapijo (3%), mnogi med njimi so bili stopnje 2 ali manj. poročali so o stomatitisu.
O slabosti in bruhanju so poročali pogosteje v kombinirani skupini (40% in 28%) kot v skupini z monoterapijo (32% in 15%); večina je bila v stopnjah resnosti 1 in 2.
Prekinitev zdravljenja z enim ali obema zdraviloma zaradi neželenih učinkov se je pojavila pri 38% bolnikov. Najpogostejši neželeni učinki, ki so privedli do prekinitve zdravljenja z bortezomibom in Caelyxom, so bili OZO, nevralgija, periferna nevropatija, periferna senzorična nevropatija, trombocitopenija, zmanjšana iztisna frakcija in utrujenost.
* palmarno-plantarna eritrodisestezija (sindrom roke-stopala).
** Neželeni učinki stopnje 3 in 4 temeljijo na neželenih učinkih vsake resnosti s "skupno incidenco ≥ 5% (glejte neželene učinke, navedene v prvem stolpcu)"
KS-AIDS : Klinične študije pri bolnikih z AIDS-KS, zdravljenih z zdravilom Caelyx v odmerku 20 mg / m2, kažejo, da je najpogostejši neželeni učinek, povezan z dajanjem zdravila Caelyx, mielosupresija, ki se pojavi tudi zelo pogosto (približno polovica bolnikov).
Levkopenija je pri tej populaciji najpogosteje zabeležen neželeni učinek pri uporabi zdravila Caelyx; poročali so o nevtropeniji, anemiji in trombocitopeniji. Ti učinki se lahko pojavijo na začetku zdravljenja. Hematološka toksičnost lahko zahteva zmanjšanje odmerka ali prekinitev ali preložitev zdravljenja. Začasno prekinite zdravljenje z zdravilom Caelyx pri bolnikih, ko je absolutno število nevtrofilcev 3 in / ali število trombocitov 3. Hematološka toksičnost pri bolnikih z rakom jajčnikov je manj huda kot pri bolnikih z AIDS-KS (glejte poglavje o bolnikih z rakom jajčnikov zgoraj).
Neželeni učinki na dihala so bili pogosto opaženi v kliničnih preskušanjih zdravila Caelyx in so lahko povezani z oportunističnimi okužbami pri bolnikih z aidsom. Pri bolnikih s KS so se po uporabi zdravila Caelyx pojavile oportunistične okužbe; takšne okužbe so pogoste pri bolnikih z imunsko pomanjkljivostjo, povzročeno s HIV. Najpogostejše oportunistične okužbe, opažene v kliničnih preskušanjih, so bile kandidoza, citomegalovirus, herpes simpleks, pljučnica Pneumocystis carinii in Mycobacterium avium kompleks.
Neželeni učinki, opaženi pri bolnikih s KS-AIDS, glede na pogostnost CIOMS III (zelo pogosti (> 1/10); pogosti (> 1/100, 1/1.000,
Okužbe in okužbe:
Pogosti: oralna moniliaza
Motnje krvnega in limfnega sistema:
Zelo pogosti: nevtropenija, anemija, levkopenija
Pogosti: trombocitopenija
Presnovne in prehranske motnje:
Pogosti: anoreksija
Psihiatrične motnje:
Občasni: zmedenost
Bolezni živčevja:
Pogosti: omotica
Občasni: parestezija
Očesne motnje:
Pogosti: retinitis
Vaskularne motnje:
Pogosti: vazodilatacija
Bolezni dihal, prsnega koša in mediastinalnega prostora:
Pogosti: dispneja
Bolezni prebavil:
Zelo pogosti: slabost
Pogosti: driska, stomatitis, bruhanje, razjede v ustih, bolečine v trebuhu, glositis, zaprtje, slabost in bruhanje
Bolezni kože in podkožja:
Pogosti: alopecija, izpuščaj
Občasni: palmarno-plantarna eritrodisestezija (OZO)
Splošne motnje in stanja na mestu aplikacije:
Pogosti: astenija, zvišana telesna temperatura, akutne reakcije, povezane z infuzijo
Diagnostični testi:
Pogosti: hujšanje
Drugi manj pogosti neželeni učinki (anafilaktične reakcije. Po trženju so pri tej populaciji redko poročali o mehurju.
Pogosto so se pojavljale klinično pomembne laboratorijske nepravilnosti (≥ 5%), ki so vključevale zvišanje alkalne fosfataze, AST in bilirubina, za katere se je štelo, da so povezane z boleznijo in ne s Caelyxom. Zmanjšanje hemoglobina in trombocitov je bilo ugotovljeno manj pogosto (virus HIV in ne v Caelyxu.
Vsi bolniki Pri 100 od 929 bolnikov (10,8%) s solidnimi tumorji so poročali o reakcijah, povezanih z infuzijo zdravila Caelyx, opredeljenimi z naslednjimi Costart indeksi: alergijska reakcija, anafilaktoidna reakcija, astma, edem obraza, hipotenzija, vazodilatacija, urtikarija, bolečine v hrbtu, bolečine v prsih, mrzlica, zvišana telesna temperatura, hipertenzija, tahikardija, dispepsija, slabost, omotica, dispneja, faringitis, izpuščaj, srbenje, znojenje, reakcije na mestu injiciranja in interakcije z zdravili. Redko (2%) poročajo o trajni prekinitvi zdravljenja. Pri podobni incidenci so v programu za raka na dojki poročali o infuzijskih reakcijah (12,4%) in primerih prekinitve zdravljenja (1,5%). Pri bolnikih z multiplim mielomom, zdravljenih s Caelyxom in bortezomibom, so o infuziji povezanih reakcij poročali s pogostnostjo 3%. Pri bolnikih z AIDS-KS so bile za reakcije, povezane z infuzijo, značilni zardevanje, zasoplost, obrazni edem, glavobol, mrzlica, bolečine v hrbtu, zategovanje v prsih in grlu in / ali hipotenzija, kar je mogoče pričakovati. - 10%. Zelo redko so opazili epileptične napade kot infuzijsko reakcijo, pri vseh bolnikih pa so se z infuzijo povezane reakcije pojavile predvsem med prvo infuzijo. Začasna prekinitev infuzije običajno odpravi te simptome brez uporabe nadaljnjega zdravljenja. Pri skoraj vseh bolnikih se lahko zdravljenje z zdravilom Caelyx nadaljuje, potem ko so vsi simptomi minili brez ponovitve. Infuzijske reakcije se po prvem zdravljenju z zdravilom Caelyx redko pojavijo (glejte poglavje 4.2).
Pri bolnikih, zdravljenih s Caelyxom, so poročali o mielosupresiji, povezani z anemijo, trombocitopenijo, levkopenijo in nevtropenijo ter redko nevtropenijo febrilnega tipa.
Stomatitis se je pojavil pri bolnikih, zdravljenih s kontinuiranimi infuzijami običajnega doksorubicinijevega klorida, in pogosto pri bolnikih, zdravljenih s Caelyxom. Stomatitis ni motil bolnikovega zaključka zdravljenja in na splošno ni zahteval prilagajanja odmerka, razen če je vplival na bolnikovo sposobnost hranjenja. V tem primeru lahko interval med odmerki podaljšate za 1-2 tedna ali zmanjšate odmerek (glejte poglavje 4.2).
Zdravljenje z doksorubicinom v dopustnih kumulativnih življenjskih odmerkih> 450 mg / m2 ali manjših odmerkih pri bolnikih s srčnimi dejavniki tveganja je povezano z večjo incidenco kongestivnega srčnega popuščanja. odmerki Caelyxa, večji od 460 mg / m2, niso pokazali kardiomiopatije, ki jo povzroča antraciklin. Priporočeni odmerek zdravila Caelyx za bolnike z AIDS-KS je 20 mg / m2 vsaka dva do tri tedne. za te bolnike z AIDS-KS (> 400 mg / m2) bi bilo potrebno več kot 20 tečajev zdravljenja z zdravilom Caelyx, kar traja 40-60 tednov.
Osem bolnikov s trdnim tumorjem, zdravljenih s kumulativnimi odmerki antraciklinov 509 mg / m2 - 1680 mg / m2, je bilo podvrženo endomiokardialni biopsiji. Ocena kardiotoksičnosti po Billinghamu je bila 0 - 1,5. Ti rezultati ustrezajo odsotnosti ali blagi srčni toksičnosti.
V veliki študiji faze III v primerjavi z doksorubicinom je 58/509 (11,4%) randomiziranih oseb (10, zdravljenih s Caelyxom v odmerku 50 mg / m2 / vsake 4 tedne v primerjavi s 48 bolniki, zdravljenimi z doksorubicinom v odmerku 60 mg / m2 / vsake 3 tedne) so izpolnjevali protokolom določena merila za srčno toksičnost med zdravljenjem in / ali spremljanjem. Srčna toksičnost je bila opredeljena kot zmanjšanje za več kot ali enako 20 točkam od vrednosti, če je počivani LVEF ostal v normalnem območju, ali kot zmanjšanje za ali večje od 10 točk, če je LVEF postal nenormalen (manjši od spodnje meje normalno). Nobeden od 10 preiskovancev, zdravljenih s Caelyxom, ki so imeli srčno toksičnost na podlagi vrednosti LVEF, ni razvil značilnih znakov in simptomov CHF. Nasprotno pa je pri 10 od 48 preiskovancev, zdravljenih z doksorubicinom, pri katerih je prišlo do srčne toksičnosti na podlagi vrednosti LVEF, razvili tudi znake in simptome CHF.
Pri bolnikih s solidnimi tumorji, vključno s subpopulacijo bolnikov z rakom dojk in jajčnikov, zdravljenih z odmerkom 50 mg / m2 / cikel s kumulativnimi odmerki antraciklina skozi celotno življenjsko dobo, to je do 1.532 mg / m2, se pojavnost klinično pomembna srčna disfunkcija je bila nizka. Od 418 bolnikov, zdravljenih s 50 mg / m2 / ciklus zdravila Caelyx in ki so bili pred zdravljenjem in vsaj enkrat med spremljanjem s pregledom MUGA nadzorovani zaradi iztisne frakcije levega prekata, je 88 bolnikov prejelo kumulativni odmerek antraciklin> 400 mg / cikel m2, stopnja izpostavljenosti, povezana s povečanim tveganjem za kardiovaskularno toksičnost pri običajnem doksorubicinu. Od teh 88 bolnikov je le 13 (15%) poročalo o vsaj eni "klinično pomembni spremembi svojega LVEF, opredeljeni kot vrednost LVEF, manjša od 45%, ali zmanjšanju za najmanj 20 točk od izhodišča. Poleg tega je le 1 bolnik (zdravljen s kumulativnim odmerkom antraciklina 944 mg / m2) je prekinil zdravljenje zaradi kliničnih simptomov kongestivnega srčnega popuščanja.
Tako kot pri drugih antineoplastičnih zdravilih, ki poškodujejo DNA, so pri bolnikih, ki so prejemali kombinirano zdravljenje z doksorubicinom, poročali o sekundarnih akutnih mieloičnih levkemijah in mielodisplaziji. Zato mora biti vsak bolnik, zdravljen z doksorubicinom, pod hematološkim nadzorom.
Zdravilo Caelyx velja za dražilno, čeprav so lokalno nekrozo po ekstravazaciji do danes opazili zelo redko. Študije na živalih kažejo, da uporaba liposomske formulacije doksorubicinijevega klorida zmanjša možnost ekstravazacijske poškodbe. Če obstajajo znaki in simptomi ekstravazacije (npr. Pekoča bolečina, eritem), takoj prekinite infuzijo in jo nadaljujte v drugačni veni. Nanos leda na mesto ekstravazacije za približno 30 minut lahko olajša reakcijo. Lokalno. Zdravila Caelyx se ne sme dajati intramuskularno ali subkutano.
Redko se lahko pri uporabi zdravila Caelyx pojavijo kožne reakcije zaradi prejšnje radioterapije.
Od trženja zdravila Caelyx so redko poročali o resnih kožnih stanjih, kot so multiformni eritem, Stevens-Johnsonov sindrom in toksična epidermalna nekroliza.
Pri bolnikih, zdravljenih s Caelyxom, so občasno opazili primere venske trombembolije, vključno s tromboflebitisom, vensko trombozo in pljučno embolijo. Ker pa je pri bolnikih z rakom povečano tveganje za nastanek trombembolične bolezni, vzročne zveze ni mogoče določiti.
04.9 Preveliko odmerjanje
Akutno preveliko odmerjanje doksorubicinijevega klorida poslabša toksične učinke mukozitisa, levkopenije in trombocitopenije. Zdravljenje akutnega prevelikega odmerjanja pri hudo mielosupresiranih bolnikih zahteva hospitalizacijo, dajanje antibiotikov, transfuzijo trombocitov in granulocitov ter simptomatsko zdravljenje mukozitisa.
05.0 FARMAKOLOŠKE LASTNOSTI
05.1 Farmakodinamične lastnosti
Farmakoterapevtska skupina: citotoksična zdravila (antraciklini in sorodne snovi), oznaka ATC: L01DB.
Zdravilna učinkovina v zdravilu Caelyx je doksorubicinijev klorid, citotoksični antibiotik iz skupine antraciklin, pridobljen iz Streptomyces peucetius var. cezij. Natančen mehanizem protitumorskega delovanja doksorubicina ni znan. Na splošno velja, da je zaviranje sinteze DNA, RNA in beljakovin glavni vzrok citotoksičnega učinka, verjetno zaradi vmešavanja antraciklina med sosednje pare baz dvojne vijačnice DNK, ki preprečuje, da bi se odvijal za replikacijo.
Naključno preskušanje faze III, v katerem so primerjali Caelyx z doksorubicinom, je vključevalo 509 bolnic z metastatskim rakom dojke. Protokolarno določen cilj dokazovanja neinferiornosti zdravila Caelyx proti doksorubicinu je bil dosežen; razmerje relativne nevarnosti (HR) do preživetja brez napredovanja bolezni (PFS) je bilo 1,00 (95% IZ za HR = 0,82-1,22) HR zdravljenje za PFS za prognostične spremenljivke so ustrezale PFS za populacijo ITT.
Primarna analiza srčne toksičnosti je pokazala, da je tveganje za nastanek srčnega dogodka v odvisnosti od kumulativnega odmerka antraciklina pri Caelyxu bistveno manjše kot pri doksorubicinu (HR = 3,16, p 2, pri Caelyxu ni prišlo do srčnih dogodkov.
Primerjalna študija Caelyxa v primerjavi s topotekanom v tretji fazi je bila zaključena pri 474 bolnikih z epitelijskim rakom jajčnikov, ki niso uspeli v prvi vrsti kemoterapije na osnovi platine. C "je bila korist celotnega preživetja (OS) pri bolnikih, zdravljenih s Caelyxom, v primerjavi s tistimi, ki so se zdravili s topotekanom, kar kaže razmerje relativne nevarnosti (HR) 1,261 (95% IZ; 1000, 1,478), P = 0,050. , 2 in 3-letno preživetje je bilo za Caelyx 56,3%, 34,7%oziroma 20,2%v primerjavi s 54,0%, 23,6%in 13,2%za Topotekan.
V podskupini bolnikov s platinsko občutljivo boleznijo je bila razlika večja: HR 1,432 (95% IZ; 1,066, 1,923), p = 0,017. Stopnja preživetja 1, 2 in 3 let je bila za Caelyx 74,1%, 51,2%oziroma 28,4%v primerjavi s 66,2%, 31,0%in 17,5%za Topotekan.
Zdravljenje je bilo podobno v podskupini bolnikov z boleznijo, ki ni občutljiva na platino: HR 1,069 (95% IZ; 0,823, 1,378), p = 0,618. Stopnja preživetja 1, 2 in 3 let je bila za Caelyx 41,5%, 21,1%oziroma 13,8%v primerjavi s 43,2%, 17,2%in 9,5%za Topotekan.
Pri 646 bolnikih z večkratnim mielomom, ki so prejeli vsaj eno predhodno terapijo in niso napredovali na terapiji na osnovi antraciklinov, so izvedli odprto, večcentrično, randomizirano, paralelno skupino, fazo III, v kateri so primerjali prenašanje in učinkovitost Kombinirano zdravljenje z zdravilom Caelyx + bortezomib v primerjavi z monoterapijo z bortezomibom.Pri bolnikih, zdravljenih s kombinirano terapijo z zdravilom Caelyx + bortezomib, je prišlo do znatnega izboljšanja v primerjavi z bolniki, ki so se zdravili samo z bortezomibom (RR ) 35% (95% IZ; 21-47%), str
05.2 Farmakokinetične lastnosti
Caelyx je dolgo krožeča, pegilirana liposomska formulacija doksorubicinijevega klorida. Pegilirani liposomi vsebujejo površinsko vezane segmente hidrofilnega polimera metoksi polietilen glikola (MPEG). Te linearne skupine se raztezajo od površine liposoma in ustvarjajo zaščitno prevleko, ki zmanjšuje interakcije med dvoslojno lipidno membrano in komponentami plazme. To omogoča, da liposomi Caelyxa dlje časa krožijo v krvi. Pegilirani liposomi so dovolj majhni (povprečni premer približno 100 nm), da nepoškodovani (z ekstravazacijo) prehajajo skozi fenestrirane kapilare, ki oskrbujejo tumorje. Dokazi o prodiranju pegiliranih liposomov iz krvnih žil ter o vstopu in kopičenju v tumorjih so bili najdeni pri miših z rakom debelega črevesa C-26 in pri transgenih miših s KS podobnimi lezijami. Za pegilirane liposome je značilna tudi nizka prepustnost lipidnega matriksa in notranji vodni puferski sistem, ki pomaga vzdrževati inkapsuliran doksorubicinijev klorid, medtem ko liposom ostane v obtoku.
Farmakokinetika Caelyxa v plazmi pri ljudeh se bistveno razlikuje od tistih, opisanih v literaturi za standardne pripravke doksorubicinijevega klorida. Pri najnižjih odmerkih (10 mg / m2 - 20 mg / m2) je za Caelyx značilna linearna farmakokinetika. mg / m2 Za Caelyx je značilna nelinearna farmakokinetika. Standardni doksorubicinijev klorid kaže znatno porazdelitev tkiva (volumen porazdelitve 700 do 1.100 l / m2) in hiter očistek (24 do 73 l / h / m2). Farmakokinetični profil zdravila Caelyx na drugi strani kaže, da ta produkt ostaja v glavnem omejen v volumnu plazme in da je očistek doksorubicina iz krvi odvisen od liposomskega transporterja. Dostopnost doksorubicina se začne po ekstravazaciji liposomov in njihov vstop v predel za tkivo.
Za enakovredne odmerke so plazemske koncentracije in AUC vrednosti Caelyxa, ki predstavljajo predvsem doksorubicinijev klorid v pegiliranih liposomih (ki vsebujejo 90% - 95% izmerjenega doksorubicina), bistveno višje od vrednosti, pridobljenih s standardnimi pripravki doksorubicinijevega klorida.
Zdravila Caelyx ne smete uporabljati zamenljivo z drugimi formulacijami doksorubicinijevega klorida.
Farmakokinetika prebivalstva
Farmakokinetiko zdravila Caelyx so pri populacijskih farmakokinetičnih pristopih ovrednotili pri 120 bolnikih iz 10 različnih kliničnih študij. model z vhodi ničelnega reda in Michealis-Mentenovo odpravo. Povprečni notranji očistek Caelyxa je bil 0,030 L / h / m2 (razpon 0,008 do 0,152 L / h / m2), srednji srednji volumen porazdelitve pa 1,93 L / m2 (razpon 0,96 do 3,85 l / m2), kar je približno prostornini plazme. Navidezni razpolovni čas je bil od 24 do 231 ur, povprečno 73,9 ure.
Bolnice z rakom dojke
Farmakokinetika zdravila Caelyx, ugotovljena pri 18 bolnikih z rakom dojke, je bila podobna farmakokinetiki, ugotovljeni pri večji populaciji 120 bolnic z različnimi vrstami raka. Povprečni notranji razmik je bil 0,016 L / h / m2 (razpon 0,008-0,027 L / h / m2), srednji volumen porazdelitve 1,46 L / m2 (razpon 1,10-1,64 L / m2). Povprečni navidezni razpolovni čas je bil 71,5 ur (razpon 45,2-98,5 ur).
Bolniki z rakom jajčnikov
Farmakokinetika zdravila Caelyx, ocenjena pri 11 bolnikih z rakom jajčnikov, je bila podobna tisti, ugotovljeni pri večji populaciji 120 bolnic z različnimi vrstami raka. Povprečni notranji razmik je bil 0,021 L / h / m2 (razpon 0,009 do 0,041 L / h / m2), srednji srednji volumen porazdelitve pa 1,95 L / m2 (razpon 1,67 do 2, 40 l / m2). Povprečni navidezni razpolovni čas je bil 75,0 ur (razpon od 36,1 do 125 ur).
Bolniki s KS-AIDS-om
Farmakokinetiko Caelyxa v plazmi so ocenjevali pri 23 bolnikih s KS, ki so jim v 30 minutah dajali enkratne odmerke 20 mg / m2 z infuzijo. Farmakokinetični parametri zdravila Caelyx (ki v prvi vrsti predstavlja doksorubicinijev klorid v pegiliranih liposomih in nizke ravni nekapsuliranega doksorubicinijevega klorida) so bili izmerjeni po dajanju 20 mg / m2 in so predstavljeni v tabeli 8.
Tabela 8. Farmakokinetični parametri pri bolnikih z AIDS-KS, zdravljenih s Caelyxom
* Izmerjeno na koncu 30 -minutne infuzije
05.3 Predklinični podatki o varnosti
Toksikološki profil zdravila Caelyx v večkratnih študijah dajanja na živalih je zelo podoben tistemu, ki so ga poročali pri dolgotrajnih infuzijah standardnega doksorubicinijevega klorida pri ljudeh.
Kardiotoksičnost : Študije, opravljene pri kuncih, so pokazale, da je kardiotoksičnost zdravila Caelyx zmanjšana v primerjavi s tisto, ki jo povzročajo običajne formulacije doksorubicinijevega klorida.
Strupenost za kožo : V študijah, izvedenih s ponavljajočo uporabo zdravila Caelyx pri podganah in psih, so pri klinično pomembnih odmerkih opazili hudo vnetje dermisa in razjede. V študiji pri psih sta se incidenca in resnost teh lezij zmanjšala z zmanjšanjem odmerka ali s podaljšanjem intervalov med odmerki. Podobne dermalne lezije, ki so opisane kot palmarno-plantarna eritrodisestezija, so opazili tudi pri bolnikih po dolgotrajni intravenski infuziji ( glejte poglavje 4.8).
Anafilaktoidni odziv : Po dajanju pegiliranih liposomov (placebo) med toksikološkimi študijami pri večkratnih odmerkih pri psih so opazili akutni odziv, za katerega so značilne hipotenzija, bledica sluznice, slinjenje, bruhanje in obdobja hiperaktivnosti, ki jim je sledila hipoaktivnost in letargija. Podoben, a manj hud odziv so opazili pri psih, zdravljenih s Caelyxom in standardnim doksorubicinom.
Intenzivnost hipotenzivnega odziva se je zmanjšala s predhodnim zdravljenjem na osnovi antihistaminikov. Vendar odziv ni ogrozil psov, ki so po prekinitvi zdravljenja hitro okrevali.
Lokalna strupenost : Študije podkožne tolerance kažejo, da Caelyx v primerjavi s standardnim doksorubicinijevim kloridom povzroči lokalno draženje ali blažjo poškodbo tkiva po možni ekstravazaciji.
Mutagenost in rakotvornost : čeprav v zvezi s tem niso bile izvedene nobene študije, je doksorubicinijev klorid, farmakološko aktivna sestavina zdravila Caelyx, mutagena in rakotvorna. Placebo pegilirani liposomi niso niti mutageni niti genotoksični.
Strupenost za razmnoževanje : Caelyx po enkratnem odmerku 36 mg / kg pri miših povzroči blago do zmerno atrofijo jajčnikov in testisov. Zmanjšana teža testisov in hipospermija sta bili prisotni pri podganah, zdravljenih s ponavljajočimi se odmerki ≥ 0,25 mg / kg / dan, in pri psih, razširjena degeneracija semenskih tubulov in izrazit upad spermatogeneze (glejte poglavje 4.6).
Nefrotoksičnost : Študija je pokazala, da "enkratna intravenska uporaba Caelyxa za več kot dvakratni klinični odmerek povzroči toksičnost za ledvice pri opicah. Toksičnost za ledvice so opazili tudi pri enkratnih nižjih odmerkih doksorubicin HCl pri podganah in kuncih. Od ocene. Globalni bolnik podatki o varnosti zdravila Caelyx v obdobju trženja niso nakazovali pomembnega trenda Caelyxa v smislu nefrotoksičnosti, podatki pri opicah morda niso pomembni za oceno tveganja za bolnike.
06.0 FARMACEVTSKE INFORMACIJE
06.1 Pomožne snovi
?- (2- [1,2-distearoil-sn-glicerofosfoksi] etilkarbamoil) -? -metoksi poli (oksietilen) -40 natrijeva sol (MPEG -DSPE)
popolnoma hidrogeniran sojin fosfatidilholin (HSPC)
holesterola
amonijev sulfat
saharoza
histidin
voda za injekcije
klorovodikova kislina
natrijev hidroksid
06.2 Nezdružljivost
Tega zdravila ne smete mešati z drugimi zdravili, razen s tistimi, ki so omenjena v poglavju 6.6.
06.3 Obdobje veljavnosti
20 mesecev
Po redčenju:
- Kemična in fizikalna stabilnost med uporabo je bila dokazana 24 ur pri temperaturah med 2 ° C in 8 ° C.
- Z mikrobiološkega vidika je treba izdelek uporabiti takoj. Če se ne uporabi takoj, so časi shranjevanja in metode razredčene raztopine pred uporabo odgovornost uporabnika in ne smejo presegati 24 ur, če so shranjene pri temperaturah med 2 ° C in 8 ° C.
- Delno uporabljene viale je treba zavreči.
06.4 Posebna navodila za shranjevanje
Shranjujte v hladilniku (2 ° C-8 ° C). Ne zamrzujte.
Za pogoje shranjevanja razredčenega zdravila glejte poglavje 6.3.
06.5 Vrsta ovojnine in vsebina pakiranja
Steklena viala tipa I s silikoniziranim sivim brombutilnim zamaškom in aluminijastim tesnilom, ki vsebuje prostornino, ki lahko odda 10 ml (20 mg) ali 25 ml (50 mg).
Caelyx je na voljo v enojnih pakiranjih ali pakiranjih po deset vial.
Na trgu ni vseh navedenih pakiranj.
06.6 Navodila za uporabo in rokovanje
Izdelka ne uporabljajte, če so prisotne oborine ali druge vrste delcev.
Z raztopino Caelyx je treba ravnati previdno. Potrebujete uporabo rokavic. Če Caelyx pride v stik s kožo ali sluznico, jih nemudoma temeljito umijte z milom in vodo. Z zdravilom Caelyx je treba ravnati v skladu z običajnimi previdnostnimi ukrepi za druga zdravila proti raku v skladu z lokalnimi predpisi.
Določite odmerek zdravila Caelyx, ki ga boste uporabili (odvisno od priporočenega odmerka in bolnikove telesne površine). S sterilno brizgo izvlecite pravilen volumen zdravila Caelyx. Delovati je treba v strogo aseptičnih pogojih, saj Caelyx ne vsebuje konzervansov ali bakteriostatikov. Pred dajanjem je treba pravilen odmerek zdravila Caelyx razredčiti v 5% raztopini glukoze (50 mg / ml) za intravensko infuzijo. Za odmerke
Uporaba razredčil, ki niso 5% raztopina glukoze (50 mg / ml) za intravensko infuzijo ali prisotnost katerega koli bakteriostatičnega sredstva, kot je benzil alkohol, lahko povzroči obarjanje Caelyxa.
Priporočljivo je, da infuzijsko linijo, ki vsebuje Caelyx, povežete s stranskim dovodom intravenske infuzije 5% glukoze (50 mg / ml). Infuzijo lahko dajemo skozi periferno veno. Ne uporabljajte z vgrajenimi filtri.
07.0 IMETNIK DOVOLJENJA ZA PROMET
Janssen Cilag International NV
Turnhoutseweg 30
B-2340 Beerse
Belgija
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET
EU/1/96/011/001
033308014
EU/1/96/011/002
033308026
EU/1/96/011/003
033308038
EU/1/96/011/004
033308040
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA
Datum prve odobritve: 21. junij 1996
Datum zadnje obnove: 19. maj 2006
10.0 DATUM REVIZIJE BESEDILA
Novembra 2010