Zdravilne učinkovine: esomeprazol
Nexium Control 20 mg gastrorezistentne tablete
Indikacije Zakaj se uporablja Nexium Control? Za kaj je to?
Zdravilo Nexium Control vsebuje zdravilno učinkovino esomeprazol. Spada v skupino zdravil, imenovanih "zaviralci protonske črpalke". Ti delujejo tako, da zmanjšajo količino kisline, ki jo proizvaja želodec.
To zdravilo se uporablja pri odraslih za kratkotrajno zdravljenje simptomov refluksa (na primer zgage in kisle regurgitacije).
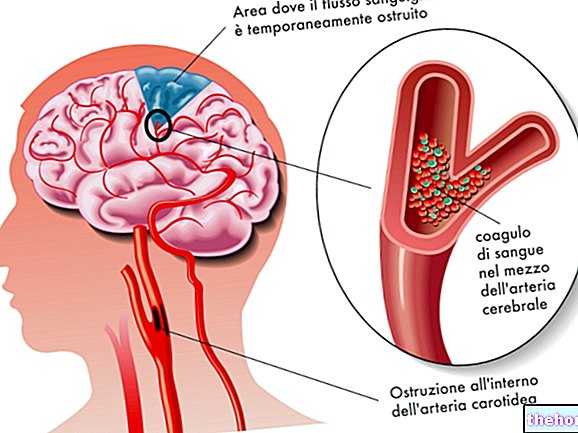
Refluks je povratni tok kisline iz želodca v požiralnik ("prehranski kanal"), ki se lahko vname in boli. To lahko povzroči simptome, kot so boleč občutek v prsih, ki se dviga v grlu (zgaga) in kisel okus v ustih (kisla regurgitacija).
Nexium Control ni zasnovan tako, da prinese takojšnje olajšanje. Morda boste morali tablete jemati 2-3 dni zapored, preden se boste počutili bolje. Če se ne počutite bolje ali če se počutite slabše po 14 dneh, se posvetujte s svojim zdravnikom.
Kontraindikacije Kadar zdravila Nexium Control ne smete uporabljati
Ne jemljite zdravila Nexium Control
- če ste alergični na esomeprazol ali katero koli sestavino tega zdravila
- če ste alergični na zdravila, ki vsebujejo druge zaviralce protonske črpalke (npr. pantoprazol, lansoprazol, rabeprazol ali omeprazol).
- če jemljete zdravilo, ki vsebuje nelfinavir (za zdravljenje okužb s HIV)
Tega zdravila ne smete jemati, če spada v katerega od zgornjih primerov. Če ste v dvomih, se pred jemanjem tega zdravila posvetujte z zdravnikom ali farmacevtom.
Previdnostni ukrepi pri uporabi Kaj morate vedeti, preden boste vzeli zdravilo Nexium Control
Preden vzamete zdravilo Nexium Control, se posvetujte s svojim zdravnikom, če:
- Imeli ste "želodčno razjedo ali že imeli operacijo želodca".
- 4 ali več tednov ste bili na zdravljenju zaradi refluksa ali zgage.
- Imate zlatenico (porumenelost kože in oči) ali hude težave z jetri.
- Imate hude težave z ledvicami.
- Stara je več kot 55 let in je imela nove ali nedavno spremenjene simptome refluksa ali potrebuje zdravila za prebavo ali zgago vsak dan brez recepta.
- Če opazite katerega od naslednjih simptomov, ki so lahko znaki druge, resnejše bolezni, se posvetujte s svojim zdravnikom.
- Hujša veliko brez razloga.
- Imate težave ali bolečine pri požiranju.
- Še posebej po jedi se pojavijo bolečine v želodcu ali znaki slabe prebave, kot so slabost, sitost, napihnjenost.
- Začne bruhati hrano ali kri, ki je lahko v bruhanju temna kot usedlina kave.
- Blato je črno (blato s krvjo).
- Imate hudo ali vztrajno drisko esomeprazol je bil povezan z majhnim povečanim tveganjem za nalezljivo drisko.
Nujno se posvetujte z zdravnikom, če čutite bolečino v prsih, ki jo spremlja omotica, znojenje, omotica ali bolečine v ramenih in težko dihanje. To je lahko simptom resne težave s srcem.
Preden vzamete to zdravilo, pokličite svojega zdravnika, če:
- Morate opraviti endoskopsko ali sečninsko preiskavo.
- Morate opraviti poseben krvni test (kromogranin A)
Če karkoli od naštetega velja za vas (ali če niste prepričani), se nemudoma obrnite na svojega zdravnika.
Otroci in mladostniki
Tega zdravila se ne sme uporabljati pri otrocih in mladostnikih, mlajših od 18 let.
Interakcije Katera zdravila ali živila lahko spremenijo učinek zdravila Nexium Control
Povejte svojemu zdravniku ali farmacevtu, če jemljete, ste pred kratkim jemali ali pa boste morda začeli jemati katero koli drugo zdravilo. To je zato, ker lahko to zdravilo vpliva na delovanje nekaterih zdravil in nekatera zdravila lahko vplivajo nanj.
Tega zdravila ne smete jemati, če jemljete tudi zdravilo, ki vsebuje nelfinavir (za zdravljenje okužbe s HIV).
Zdravniku ali farmacevtu morate povedati, če jemljete klopidogrel (za preprečevanje nastajanja krvnih strdkov).
Tega zdravila ne smete jemati z drugimi zdravili, ki omejujejo količino kisline, ki nastaja v želodcu, kot so zaviralci protonske črpalke (npr. Pantoprazol, lansoprazol, rabeprazol ali omeprazol) ali antagonisti H2 (npr. Ranitidin ali famotidin).
Po potrebi lahko to zdravilo jemljete z antacidi (npr. Magaldrat, alginska kislina, natrijev bikarbonat, aluminijev hidroksid, magnezijev karbonat ali njihove kombinacije).
Povejte svojemu zdravniku ali farmacevtu, če jemljete katero od naslednjih zdravil:
- Ketokonazol in itrakonazol (uporabljata se za zdravljenje glivičnih okužb)
- Vorikonazol (za zdravljenje okužb, ki jih povzroča gliva) in klaritromicin (za zdravljenje okužb). Zdravnik vam bo morda prilagodil odmerek zdravila Nexium Control, če imate tudi hude težave z jetri in se dalj časa zdravite.
- Erlotinib (uporablja se za zdravljenje raka)
- Metotreksat (uporablja se za zdravljenje raka in revmatičnih bolezni)
- Digoksin (uporablja se pri težavah s srcem)
- Atazanavir, sakvinavir (uporablja se za zdravljenje okužbe s HIV)
- Citalopram, imipramin ali klomipramin (za zdravljenje depresije)
- Diazepam (uporablja se za zdravljenje tesnobe, za sprostitev mišic ali pri epilepsiji)
- Fenitoin (uporablja se za zdravljenje epilepsije)
- Zdravila za redčenje krvi, na primer varfarin. Zdravnik vas bo morda moral spremljati, ko začnete ali prekinite zdravljenje z zdravilom Nexium Control
- Cilostazol (uporablja se za zdravljenje občasne klavdikacije - stanje, pri katerem slaba oskrba s krvjo v mišicah nog povzroča bolečine in težave pri hoji)
- Cisaprid (uporablja se za prebavne motnje in zgago)
- Rifampicin (uporablja se za zdravljenje tuberkuloze)
- Takrolimus (v primeru presaditve organa)
- Šentjanževka (Hypericum perforatum) (uporablja se za zdravljenje depresije)
Opozorila Pomembno je vedeti, da:
Nosečnost in dojenje
Kot previdnostni ukrep se raje izogibajte uporabi zdravila Nexium Control med nosečnostjo.Tega zdravila ne smete uporabljati med dojenjem.
Če ste noseči ali dojite, menite, da bi lahko bili noseči ali načrtujete zanositev, se pred jemanjem tega zdravila posvetujte z zdravnikom ali farmacevtom.
Vpliv na sposobnost upravljanja vozil in strojev
Nexium Control ima majhno verjetnost, da bi vplival na sposobnost vožnje in upravljanja s stroji. Neželeni učinki, kot sta omotica in motnje vida, so občasni (glejte poglavje 4). Če se pojavijo, ne vozite in ne upravljajte strojev.
Nexium Control vsebuje saharozo
Nexium Control vsebuje sladkorne krogle, ki vsebujejo saharozo, vrsto sladkorja. Če vam je zdravnik povedal, da imate intoleranco za nekatere sladkorje, se pred jemanjem zdravila posvetujte z zdravnikom.
Odmerek, način in čas dajanja Kako uporabljati Nexium Control: Odmerjanje
Pri jemanju tega zdravila natančno upoštevajte navodila v tem navodilu ali navodila zdravnika ali farmacevta. Če ste v dvomih, se posvetujte z zdravnikom ali farmacevtom.
Koliko vzeti
- Priporočeni odmerek je ena tableta na dan.
- Ne vzemite več kot priporočeni odmerek ene tablete (20 mg) na dan, tudi če ne čutite takojšnjega izboljšanja.
- Tablete boste morda morali jemati dva ali tri zaporedne dni, preden se simptomi refluksa (na primer zgaga in kisla regurgitacija) izboljšajo.
- Trajanje zdravljenja je do 14 dni.
- Ko simptomi refluksa popolnoma izginejo, morate prenehati jemati to zdravilo.
- Če se vaši simptomi refluksa poslabšajo ali se ne izboljšajo po 14 dneh zaporednega jemanja tega zdravila, se morate posvetovati z zdravnikom.
Če se tudi po zdravljenju s tem zdravilom pogosto pojavljajo trajni ali dolgotrajni ponavljajoči se simptomi, se obrnite na svojega zdravnika.
Jemanje zdravila
- Tableto lahko vzamete kadar koli čez dan s hrano ali na tešče.
- Tableto pogoltnite celo s kozarcem vode. Tablete ne žvečite ali zdrobite. To je zato, ker tableta vsebuje obložene granule, ki ščitijo zdravilo pred želodčno kislino, zato je pomembno, da zrnc ne poškodujete.
Alternativna metoda jemanja zdravila
- Tableto dajte v kozarec negazirane (negazirane) vode. Ne uporabljajte drugih tekočin.
- Mešajte, dokler se tableta ne raztopi (zmes ne bo bistra), nato pa mešanico popijte takoj ali v 30 minutah. Mešanico vedno premešajte tik pred pitjem.
- Če želite zagotoviti, da ste popili vse zdravilo, steklo temeljito sperite s pol kozarca vode in popijte. Trdni delci vsebujejo zdravilo - ne žvečite ga ali ga drobite.
Preveliko odmerjanje Kaj storiti, če ste vzeli preveč zdravila Nexium Control
Če ste vzeli večji odmerek zdravila Nexium Control, kot bi smeli
Če ste vzeli večji odmerek zdravila Nexium Control, kot je priporočeno, takoj obvestite svojega zdravnika ali farmacevta. Lahko se pojavijo simptomi, kot so driska, bolečine v trebuhu, zaprtje, občutek ali slabost in utrujenost.
Če ste pozabili vzeti zdravilo Nexium Control
Če ste pozabili vzeti odmerek, ga vzemite takoj, ko se spomnite na isti dan. Ne vzemite dvojnega odmerka, če ste pozabili vzeti prejšnji odmerek. Če imate dodatna vprašanja o uporabi tega zdravila, se posvetujte z zdravnikom ali farmacevtom.
Neželeni učinki Kakšni so stranski učinki zdravila Nexium Control
Kot vsa zdravila ima lahko tudi to zdravilo neželene učinke, ki pa se ne pojavijo pri vseh bolnikih.
Če opazite katerega od naslednjih resnih neželenih učinkov, prenehajte jemati zdravilo Nexium Control in se nemudoma posvetujte z zdravnikom:
- Nenadno piskanje, otekanje ustnic, jezika in grla, izpuščaj, omedlevica ali težave pri požiranju (huda alergijska reakcija, redko opažena).
- Pordelost kože z mehurji ali luščenjem. Močni mehurji in krvavitve se lahko pojavijo tudi na ustnicah, očeh, ustih, nosu in genitalijah. To je lahko "Stevens-Johnsonov sindrom" ali "strupena epidermalna nekroliza", ki se pojavita zelo redko.
- Redko opazimo rumeno kožo, temen urin in utrujenost, ki so lahko simptomi težav z jetri.
Čim prej se posvetujte z zdravnikom, če imate katerega od naslednjih znakov okužbe:
To zdravilo v zelo redkih primerih vpliva na bele krvničke, kar vodi v imunsko pomanjkljivost. Če imate "okužbo s simptomi, kot je zvišana telesna temperatura s hudim poslabšanjem splošnega zdravja ali zvišana telesna temperatura s simptomi lokalne okužbe, kot so bolečine v vratu, grlu ali ustih ali težave pri uriniranju, se morate čim prej posvetovati z zdravnikom, da pomanjkanje belih krvnih celic (agranulocitoza) je mogoče izključiti z izvedbo krvnega testa, v tem primeru je pomembno, da zdravniku poveste o zdravilu, ki ga jemljete.
Drugi neželeni učinki vključujejo:
Pogosti (pojavijo se lahko pri največ 1 od 10 bolnikov)
- Glavobol.
- Učinki na želodec ali črevesje: driska, bolečine v želodcu, zaprtje, veter (napenjanje).
- Slabost (slabost) ali slabost (bruhanje).
Občasni (pojavijo se lahko pri največ 1 od 100 bolnikov)
- Otekanje stopal in gležnjev.
- Moten spanec (nespečnost), zaspanost.
- Vrtoglavica, mravljinčenje kot "ščepci".
- Občutek vrtenja (vrtoglavica).
- Suha usta
- Spremembe krvnih preiskav, ki preverjajo delovanje jeter.
- Kožni izpuščaj, kožni izcedek (koprivnica) in srbeča koža.
Redki (pojavijo se pri največ 1 od 1.000 bolnikov)
- Težave s krvjo, kot je zmanjšano število belih krvnih celic ali trombocitov. To lahko povzroči šibkost, podplutbe ali možnost lažje okužbe.
- Nizke ravni natrija v krvi. To lahko povzroči šibkost, slabost (bruhanje) in krče.
- Občutek vznemirjenosti, zmedenosti ali depresije.
- Spremembe okusa.
- Težave z vidom, kot je zamegljen vid.
- Nenadno piskanje ali težko dihanje (bronhospazem).
- Vnetje v ustih.
- Okužba, imenovana "drozd", ki lahko prizadene črevesje in jo povzroči gliva.
- Izpadanje las (alopecija).
- Kožni izpuščaj pri izpostavljenosti soncu.
- Bolečine v sklepih (artralgija) ali bolečine v mišicah (mialgija).
- Splošen občutek slabosti in pomanjkanja moči.
- Povečano potenje.
Zelo redki (pojavijo se pri največ 1 od 10.000 ljudi)
- Nizko število rdečih krvnih celic, belih krvnih celic in trombocitov (stanje, imenovano pancitopenija).
- Agresija.
- Videti, občutiti ali slišati stvari, ki jih ni (halucinacije).
- Hude težave z jetri, ki vodijo v odpoved jeter in vnetje možganov. ? Mišična šibkost.
- Hude težave z ledvicami.
- Povečanje prsi pri moških.
Neznana (pogostnosti iz razpoložljivih podatkov ni mogoče oceniti)
- Nizke ravni magnezija v krvi. To lahko povzroči utrujenost, slabo počutje (bruhanje), nehoteno krčenje mišic, tresenje in spremembe srčnega ritma (aritmija). Če imate zelo nizko raven magnezija, se lahko pojavijo tudi nizke ravni kalcija in / ali kalija v krvi.
- Vnetje črevesja (ki lahko povzroči drisko).
Poročanje o stranskih učinkih
Če opazite kateri koli neželeni učinek, se posvetujte z zdravnikom ali farmacevtom, kar vključuje morebitne neželene učinke, ki niso navedeni v tem navodilu.
O neželenih učinkih lahko poročate tudi neposredno prek nacionalnega sistema poročanja, navedenega v Dodatku V. S poročanjem o neželenih učinkih lahko pomagate zagotoviti več informacij o varnosti tega zdravila.
Potek in hramba
Zdravilo shranjujte nedosegljivo otrokom!
Tega zdravila ne smete uporabljati po datumu izteka roka uporabnosti, ki je naveden na škatli in pretisnem omotu poleg oznake EXP / EXP. Rok uporabnosti se nanaša na zadnji dan navedenega meseca. Shranjujte pri temperaturi do 30 ° C.
Zdravilo shranjujte v originalni ovojnini, da ga zaščitite pred vlago.
Ne mečite nobenih zdravil v odpadne vode ali med gospodinjske odpadke. Vprašajte svojega farmacevta, kako zavreči zdravila, ki jih ne uporabljate več. Tako boste zaščitili okolje.
Vsebina pakiranja in druge informacije
Kaj vsebuje zdravilo Nexium Control
- Zdravilna učinkovina je esomeprazol. Ena tableta vsebuje 20 mg esomeprazola (v obliki magnezijevega trihidrata).
- Pomožne snovi so: glicerol monostearat 40-55, hiproloza, hipromeloza, železov oksid (rdeče-rjav E 172), železov oksid (rumeni E172), magnezijev stearat, kopolimer etil akrilata metakrilne kisline (1: 1) disperzija pri 30%, mikrokristalna celuloza, sintetični parafin, makrogol 6000, polisorbat 80, krospovidon (tip A), natrijev stearil fumarat, kroglice sladkorja (saharoza), smukec, titanov dioksid (E 171) in trietil citrat.
Izgled zdravila Nexium Control in vsebina pakiranja
Gastrorezistentne tablete Nexium Control so svetlo rožnate, podolgovate, bikonveksne z oznako "20 mg" na eni strani in A / EH na drugi strani.
Nexium Control je na voljo v pretisnih omotih po 7 in 14 gastrorezistentnih tablet.
Na trgu ni vseh navedenih pakiranj.
Navodilo za uporabo vira: AIFA (Italijanska agencija za zdravila). Vsebina, objavljena januarja 2016. Prisotne informacije morda niso posodobljene.
Za dostop do najnovejše različice je priporočljivo dostopati do spletnega mesta AIFA (Italijanska agencija za zdravila). Zavrnitev odgovornosti in koristne informacije.
01.0 IME ZDRAVILA
NEXIUM CONTROL 20 MG HRANILNO ODporne tablice
02.0 KAKOVOSTNA IN KOLIČINSKA SESTAVA
Vsaka gastrorezistentna tableta vsebuje 20 mg esomeprazola (v obliki magnezijevega trihidrata).
Pomožne snovi z znanim učinkom:
Vsaka gastrorezistentna tableta vsebuje 28 mg saharoze.
Za celoten seznam pomožnih snovi glejte poglavje 6.1.
03.0 FARMACEVTSKA OBLIKA
Gastro odporna tableta.
Svetlo roza, podolgovata, bikonveksna, filmsko obložena tableta z oznako "20 mg" na eni strani in A / EH na drugi strani.
04.0 KLINIČNE INFORMACIJE
04.1 Terapevtske indikacije
Nexium Control je indiciran pri odraslih za kratkotrajno zdravljenje simptomov refluksa (npr. Zgaga in kisla regurgitacija).
04.2 Odmerjanje in način uporabe
Odmerjanje
Priporočeni odmerek je 20 mg esomeprazola (ena tableta) na dan.
Za izboljšanje simptomov bo morda treba jemati tablete 2-3 dni zapored. Trajanje zdravljenja je do 2 tedna. Ko simptomi popolnoma izginejo, je treba zdravljenje prekiniti.
Če simptomi ne izzvenijo v 2 tednih neprekinjenega zdravljenja, se mora bolnik posvetovati z zdravnikom.
Posebne populacije
Bolniki z okvaro ledvic
Pri bolnikih z okvarjenim delovanjem ledvic prilagoditev odmerka ni potrebna. Zaradi omejenih izkušenj pri bolnikih s hudo ledvično insuficienco je treba takšne bolnike zdraviti previdno (glejte poglavje 5.2).
Bolniki z okvaro jeter
Pri bolnikih z blago do zmerno okvaro jeter prilagajanje odmerka ni potrebno. Vendar pa mora bolnike s hudo okvaro jeter zdravnik svetovati, preden vzamejo zdravilo Nexium Control (glejte poglavji 4.4 in 5.2).
Starejši bolniki (stari ≥ 65 let)
Pri starejših bolnikih prilagoditev odmerka ni potrebna.
Pediatrična populacija
Ni indikacij za posebno uporabo zdravila NEXIUM Control pri pediatrični populaciji, mlajši od 18 let, pri indikaciji: "kratkotrajno zdravljenje simptomov refluksa (npr. Zgaga in kisla regurgitacija)".
Način dajanja
Tablete je treba pogoltniti cele s pol kozarca vode. Tablet ne smete žvečiti ali drobiti.
Druga možnost je, da tableto razpršite v pol kozarca negazirane vode. Ne uporabljajte drugih tekočin, ker se lahko gastrorezistentna obloga raztopi. Vodo je treba mešati, dokler se tableta ne razprši. Tekočino z granulami je treba popiti takoj ali v 30 minutah. Kozarec je treba sprati s pol kozarca vode in pitne vode. Zrnca se ne smejo žvečiti ali drobiti.
04.3 Kontraindikacije
Preobčutljivost za esomeprazol, nadomestke benzimidazola ali katero koli pomožno snov (glejte poglavje 6.1).
Esomeprazola se ne sme uporabljati sočasno z nelfinavirjem (glejte poglavje 4.5).
04.4 Posebna opozorila in ustrezni previdnostni ukrepi za uporabo
Splošno
Bolnikom je treba naročiti, naj se posvetujejo z zdravnikom, če:
• Imate znatno nenamerno izgubo telesne mase, ponavljajoče se bruhanje, disfagijo, hematemezo ali melano, in če obstaja sum ali prisotnost želodčne razjede, je treba izključiti maligno naravo razjede, saj lahko zdravljenje z esomeprazolom ublaži simptome in odloži diagnozo.
• ste imeli predhodno želodčno razjedo ali operacijo prebavil.
• 4 ali več tednov ste bili na stalnem simptomatskem zdravljenju dispepsije ali zgage.
• če imate zlatenico ali hudo bolezen jeter.
• ste starejši od 55 let z novimi ali nedavno spremenjenimi simptomi.
Bolniki z dolgotrajnimi ponavljajočimi se simptomi dispepsije ali zgage morajo redno obiskovati svojega zdravnika. Zlasti morajo bolniki, starejši od 55 let, ki se dnevno zdravijo zaradi dispepsije in zgage brez recepta, obvestiti svojega zdravnika ali farmacevta.
Bolniki ne smejo jemati zdravila Nexium Control kot dolgoročno preventivno zdravilo.
Zdravljenje z zaviralci protonske črpalke (IPČ) lahko nekoliko poveča tveganje za okužbe prebavil, na primer tiste izSalmonela In Campylobacter, in morda tudi iz Clostridium difficile pri hospitaliziranih bolnikih (glejte poglavje 5.1).
Bolniki se morajo pred jemanjem tega zdravila posvetovati s svojim zdravnikom, če bodo opravili endoskopsko preiskavo ali test sečnine.
Kombinacija z drugimi zdravili
Sočasna uporaba esomeprazola in atazanavirja ni priporočljiva (glejte poglavje 4.5). Če je kombinacija atazanavirja z zaviralcem protonske črpalke neizogibna, je priporočljivo skrbno klinično spremljanje v povezavi s povečanjem odmerka atazanavirja na 400 mg s 100 mg ritonavirja. Odmerka 20 mg esomeprazola ne smemo preseči.
Esomeprazol je zaviralec CYP2C19. Na začetku ali koncu zdravljenja z esomeprazolom je treba razmisliti o možni interakciji z zdravili, ki se presnavljajo s CYP2C19. Med klopidogrelom in esomeprazolom so opazili medsebojno delovanje, klinični pomen te interakcije je negotov, zato je treba uporabo esomeprazola in klopidogrela odsvetovati (glejte poglavje 4.5).
Bolniki ne smejo jemati drugih antagonistov IPČ ali H2 hkrati.
Saharoza
To zdravilo vsebuje sladkorne krogle (saharozo). Bolniki z redko dedno intoleranco za fruktozo, malabsorpcijo glukoze-galaktoze ali pomanjkanjem saharaze-izomaltaze ne smejo jemati tega zdravila.
Vpliv na laboratorijske teste
Povišana raven kromogranina A (CgA) lahko vpliva na preiskave nevroendokrinih tumorjev. Da bi se izognili temu motenju, je treba zdravljenje z esomeprazolom začasno prekiniti pet dni pred določitvijo CgA.
04.5 Interakcije z drugimi zdravili in druge oblike interakcij
Študije interakcij so bile izvedene samo pri odraslih.
Vpliv esomeprazola na farmakokinetiko drugih zdravil
Ker je esomeprazol enantiomer omeprazola, je priporočljivo upoštevati interakcije, opažene z omeprazolom.
Zaviralci proteaz
Poročali so o medsebojnem delovanju med omeprazolom in nekaterimi zaviralci proteaz. Klinični pomen in mehanizmi teh interakcij niso vedno znani. Povečanje želodčnega pH med zdravljenjem z omeprazolom lahko spremeni absorpcijo zaviralcev proteaz.Drugi možni mehanizmi interakcije se pojavijo z zaviranjem CYP2C19.
Pri atazanavirju in nelfinavirju so pri jemanju z omeprazolom poročali o znižanih koncentracijah v serumu, zato sočasna uporaba ni priporočljiva. Sočasna uporaba omeprazola (40 mg enkrat na dan) s 300 mg atazanavirja / 100 mg ritonavirja pri zdravih prostovoljcih povzroči znatno zmanjšanje izpostavljenosti atazanavirju (približno 75% zmanjšanje AUC, Cmax in Cmin). Povečanje odmerka atazanavirja na 400 mg ne kompenzira vpliva omeprazola na izpostavljenost atazanavirju. Sočasna uporaba omeprazola (20 mg enkrat na dan (qd)) s 400 mg atazanavirja / 100 mg ritonavirja pri zdravih prostovoljcih je povzročila približno 30-odstotno zmanjšanje izpostavljenosti atazanavirju v primerjavi z izpostavljenostjo, opaženo pri atazanavirju 300 mg / ritonavirju 100 mg na dan brez omeprazola 20 mg na dan. Sočasna uporaba omeprazola (40 mg na dan) je zmanjšala "AUC, povprečno Cmax in Cmin nelfinavirja za 36- 39% in "AUC, povprečni Cmax in Cmin farmakološko aktivnega presnovka M8 so se zmanjšali za 75-92%. Zaradi farmakodinamičnih učinkov in podobnih farmakokinetičnih lastnosti omeprazola in esomeprazola sočasna uporaba esomeprazola in atazanavirja ni priporočljiva, sočasna uporaba pa esomeprazol in nelfinavir sta kontraindicirana (glejte poglavji 4.3 in 4.4).
Med sočasnim zdravljenjem z omeprazolom (40 mg na dan) so poročali o zvišanih koncentracijah sakvinavirja (80-100%) (sočasno z ritonavirjem). Zdravljenje z 20 mg omeprazola enkrat na dan ni vplivalo na izpostavljenost darunavirju (sočasno z ritonavirjem) in amprenavirju (sočasno dajanje z ritonavirjem).
Zdravljenje z 20 mg esomeprazola enkrat na dan ni vplivalo na izpostavljenost amprenavirju (z in brez sočasne uporabe z ritonavirjem). Zdravljenje z omeprazolom v odmerku 40 mg enkrat na dan ni vplivalo na izpostavljenost lopinavirju (pri sočasni uporabi z ritonavirjem)
Metotreksat
Pri nekaterih bolnikih so poročali o zvišanju ravni metotreksata v kombinaciji z IPČ. V prisotnosti velikih odmerkov metotreksata bo morda treba razmisliti o začasni prekinitvi esomeprazola.
Takrolimus
Pri sočasni uporabi esomeprazola in takrolimusa so poročali o zvišanih koncentracijah takrolimusa v serumu. Okrepiti je treba koncentracijo takrolimusa in delovanje ledvic (očistek kreatinina) ter po potrebi prilagoditi odmerek takrolimusa.
Zdravila z absorpcijo, odvisno od pH
Zatiranje želodčne kislosti med zdravljenjem z esomeprazolom in drugimi PPI lahko zmanjša ali poveča absorpcijo zdravil s pH, odvisno od absorpcije želodca. Absorpcija zdravil, kot so ketokonazol, itrakonazol in erlotinib, se lahko med zdravljenjem z esomeprazolom zmanjša, absorpcija digoksina pa se lahko poveča med zdravljenjem z esomeprazolom.
Sočasno zdravljenje z omeprazolom (20 mg na dan) in digoksinom pri zdravih osebah je povečalo biološko uporabnost digoksina za 10% (do 30% pri dveh od desetih oseb). Redko so poročali o toksičnosti digoksina. Pri dajanju esomeprazola v velikih odmerkih starejšim bolnikom je potrebna previdnost, zato je treba okrepiti spremljanje terapevtskega učinka digoksina.
Zdravila, ki se presnavljajo s CYP2C19
Esomeprazol zavira CYP2C19, glavni encim za presnovo esomeprazola. Zato se lahko v kombinaciji z esomeprazolom z drugimi zdravili, ki se presnavljajo prek CYP2C19, kot so varfarin, fenitoin, citalopram, imipramin, klomipramin, diazepam itd., Lahko povečajo plazemske koncentracije teh zdravil in bo morda treba zmanjšati odmerek. v primeru klopidogrela, predzdravila, ki ga CYP2C19 pretvori v aktivni presnovek, se lahko koncentracija aktivnega presnovka v plazmi zmanjša.
Varfarin
Sočasna uporaba 40 mg esomeprazola pri bolnikih, ki so v klinični študiji prejemali varfarin, je pokazala, da časi strjevanja ostajajo v normalnih mejah. Vendar so v obdobju trženja med sočasnim zdravljenjem poročali o nekaterih izoliranih primerih povišanih vrednosti INR, ki so klinično pomembne. Priporočeno je spremljanje na začetku in koncu sočasnega zdravljenja z esomeprazolom med zdravljenjem z varfarinom ali drugimi derivati kumarina.
Klopidogrel
Rezultati študij pri zdravih prostovoljcih so pokazali farmakokinetično (PK) / farmakodinamično (PD) interakcijo med klopidogrelom (300 mg polnilni odmerek / 75 mg dnevni vzdrževalni odmerek) in esomeprazolom (40 mg peroralno dnevno), kar je povzročilo zmanjšano izpostavljenost aktivnemu presnovku klopidogrela v povprečju 40%, kar ima za posledico zmanjšanje največje inhibicije agregacije trombocitov (induciran ADP) v povprečju 14%.
V študiji pri zdravih osebah so opazili skoraj 40 -odstotno zmanjšanje izpostavljenosti aktivnemu presnovku klopidogrela pri uporabi fiksne kombinacije esomeprazola 20 mg + ASA 81 mg in klopidogrela v primerjavi s samim klopidogrelom. najvišje ravni zaviranja agregacije trombocitov (induciran ADP) so bile v obeh skupinah enake.
Poročali so o edinstvenih podatkih iz opazovalnih in kliničnih študij o kliničnih posledicah te interakcije PK / PD v smislu velikih srčno-žilnih dogodkov. Previdnostno je treba sočasno uporabo esomeprazola in klopidogrela odsvetovati.
Fenitoin
Sočasna uporaba 40 mg esomeprazola povzroči 13 -odstotno povečanje najnižje plazemske ravni fenitoina pri bolnikih z epilepsijo. Ko začnete ali prekinite zdravljenje z esomeprazolom, je priporočljivo spremljati plazemske koncentracije fenitoina.
Vorikonazol
Omeoprazol (40 mg enkrat na dan) je povečal Cmax in AUC vorikonazola (substrat CYP2C19) za 15% oziroma 41%.
Cilostazol
Omeoprazol in esomeprazol delujeta kot zaviralca CYP2C19. Omeprazol, ki je bil v navzkrižni študiji dan v odmerkih 40 mg pri zdravih osebah, je povečal Cmax in AUC cilostazola za 18% oziroma 26%, enega od njegovih aktivnih presnovkov pa za 29% oziroma 69%.
Cisaprid
Pri zdravih prostovoljcih je sočasna uporaba 40 mg esomeprazola povzročila 32% povečanje površine pod krivuljo plazemske koncentracije / časa (AUC) in 31% podaljšanje razpolovnega časa (t1 / 2), vendar ne bistveno povečanje najvišje plazemske koncentracije cisaprida. Rahlo podaljšanje intervala QTc, opaženo po uporabi samo cisaprida, se ne podaljša, če se cisaprid daje v kombinaciji z esomeprazolom.
Diazepam
Sočasna uporaba 30 mg esomeprazola je povzročila 45 -odstotno zmanjšanje očistka diazepama substrata CYP2C19.
Študirana zdravila brez pomembnih kliničnih interakcij
Amoksicilin in kinidin
Pokazalo se je, da esomeprazol nima klinično pomembnega učinka na farmakokinetiko amoksicilina in kinidina.
Naproksen ali rofekoksib
Študije, ki so ocenjevale sočasno uporabo esomeprazola z naproksenom ali rofekoksibom, v kratkotrajnih študijah niso pokazale klinično pomembnih farmakokinetičnih interakcij.
Vpliv drugih zdravil na farmakokinetiko esomeprazola
Zdravila, ki zavirajo CYP2C19 in / ali CYP3A4
Esomeprazol se presnavlja s CYP2C19 in CYP3A4. Sočasno zdravljenje esomeprazola z zaviralcem CYP3A4, klaritromicinom (500 mg dvakrat na dan (dvakrat na dan)) povzroči podvojitev izpostavljenosti (AUC) esomeprazolu. Sočasna uporaba esomeprazola in kombiniranega zaviralca CYP2C19 in CYP3A4 lahko povzročita več kot podvojeno izpostavljenost esomeprazolu. Vorikonazol, zaviralec CYP2C19 in CYP3A4, poveča AUC omeprazola za 280%. Prilagoditev odmerka esomeprazola rutinsko ni potrebna v nobeni od zgoraj navedenih situacij. Pri bolnikih s hudo jetrno okvaro in če je indicirano dolgotrajno zdravljenje, je treba razmisliti o prilagoditvi odmerka.
Zdravila, ki inducirajo CYP2C19 in / ali CYP3A4
Zdravila, za katera je znano, da inducirajo CYP2C19 ali CYP3A4 ali oboje (na primer rifampicin in šentjanževka (Hypericum perforatum)), lahko povzročijo znižanje ravni esomeprazola v serumu zaradi povečane presnove esomeprazola.
04.6 Nosečnost in dojenje
Nosečnost
Skromna količina podatkov o nosečnicah (med 300–1000 izidi nosečnosti) kaže na to, da esomeprazol ni malformacij ali strupenosti za plod / novorojenčka.
Študije na živalih ne kažejo neposrednih ali posrednih škodljivih učinkov na sposobnost razmnoževanja (glejte poglavje 5.3).
Kot previdnostni ukrep se je priporočljivo izogibati uporabi zdravila Nexium Control med nosečnostjo.
Čas hranjenja
Ni znano, ali se esomeprazol / njegovi presnovki izločajo v materino mleko. Ni podatkov o učinkih esomeprazola na novorojenčke / dojenčke. Esomeprazola se ne sme uporabljati med dojenjem.
Plodnost
Študije na živalih z racemno mešanico omeprazola, dane peroralno, ne kažejo vpliva na plodnost.
04.7 Vpliv na sposobnost vožnje in upravljanja s stroji
Esomeprazol rahlo vpliva na sposobnost vožnje in upravljanja s stroji. Neželeni učinki, kot so omotica in motnje vida, so občasni (glejte poglavje 4.8). Ob prisotnosti teh simptomov bolniki ne smejo voziti avtomobila in upravljati strojev.
04.8 Neželeni učinki
Povzetek varnostnega profila
Glavobol, bolečine v trebuhu, driska in slabost so med najpogosteje prijavljenimi neželenimi učinki v kliničnih preskušanjih (in tudi pri uporabi po dajanju zdravila v promet). Poleg tega je varnostni profil podoben za različne formulacije, indikacije zdravljenja, skupine. Starost in populacijo bolnikov št. ugotovljeni neželeni učinki, povezani z odmerkom.
Tabela neželenih učinkov
Med kliničnimi preskušanji z esomeprazolom in v obdobju trženja so ugotovili ali domnevali naslednje neželene učinke. Reakcije so bile razvrščene po konvenciji MedDRA o pogostosti: zelo pogoste> 1/10; pogosti ≥ 1/100,
Poročanje o domnevnih neželenih učinkih
Poročanje o domnevnih neželenih učinkih, ki se pojavijo po pridobitvi dovoljenja za promet z zdravilom, je pomembno, saj omogoča stalno spremljanje razmerja med koristjo in tveganjem zdravila. spletna stran: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Preveliko odmerjanje
Trenutno obstajajo "zelo omejene" izkušnje o namernem prevelikem odmerjanju. Simptomi, opisani v povezavi z vnosom 280 mg, so bili gastrointestinalni simptomi in šibkost. Enkratni odmerek 80 mg esomeprazola ni povzročil nobenih posledic. Poseben protistrup ni znan. Esomeprazol se v veliki meri veže na beljakovine v plazmi in se zato ne more hitro dializirati. Zdravljenje mora biti simptomatsko in na splošno je treba uporabiti podporne ukrepe.
05.0 FARMAKOLOŠKE LASTNOSTI
05.1 Farmakodinamične lastnosti
Farmakoterapevtska skupina: zdravila za motnje, povezane s kislino, zaviralci kislinske črpalke, oznaka ATC: A02BC05.
Esomeprazol je izomer S omeprazola in zmanjšuje izločanje želodčne kisline s posebnim ciljnim mehanizmom delovanja.Esomeprazol je specifičen zaviralec kislinske črpalke v parietalni celici. Tako R kot S izomera omeprazola imata podobno farmakodinamično aktivnost.
Mehanizem delovanja
Esomeprazol je šibka baza in se koncentrira in pretvori v aktivno obliko v zelo kislem okolju sekretornih kanalčkov parietalne celice, kjer zavira encim črpalke kisline H + K + - ATPaza in zavira tako bazalno kot stimulirano izločanje kisline .
Farmakodinamični učinki
Po peroralnem dajanju esomeprazola v odmerku 20 mg in 40 mg se učinek pojavi v eni uri. 7 ur po petem dnevnem odmerku.
Po petih dneh peroralne uporabe z 20 mg in 40 mg esomeprazola se intragastrični pH vzdržuje na vrednosti nad 4 v povprečju 13 oziroma 17 ur od 24 pri bolnikih s simptomatsko gastroezofagealno refluksno boleznijo (GERB) . Delež bolnikov, ki so vzdrževali intragastrični pH nad 4 vsaj 8, 12 in 16 ur, je bil pri 20 mg esomeprazola 76%, 54% oziroma 24%. Ustrezne vrednosti za 40 mg esomeprazola so bile 97%, 92%in 56%.
Z uporabo AUC kot nadomestnega parametra za plazemsko koncentracijo je bila dokazana korelacija med zaviranjem izločanja kisline in izpostavljenostjo zdravilu.
Med zdravljenjem z antisekretornimi zdravili se raven gastrina v serumu poveča kot odgovor na zmanjšano izločanje kisline. Raven CgA se poveča tudi zaradi zmanjšane kislosti želodca.
Pri dolgotrajnem zdravljenju z esomeprazolom so pri nekaterih bolnikih opazili povečanje števila celic ECL, ki je verjetno povezano z zvišanjem ravni gastrina v serumu.
Zmanjšanje želodčne kislosti iz kakršnega koli razloga, vključno z zaviralci zaviralne kisline, poveča bakterijsko obremenitev želodca z bakterijami, ki so običajno prisotne v prebavnem traktu. SalmonelaIn Campylobacter in morda tudi iz Clostridium difficile pri hospitaliziranih bolnikih.
Klinična učinkovitost
20 mg esomeprazola se je izkazalo za učinkovito pri zdravljenju pogoste zgage pri osebah, ki so prejemale odmerek vsakih 24 ur 2 tedna. V dveh ključnih, multicentričnih, randomiziranih, dvojno slepih, s placebom nadzorovanih študijah je bilo 234 oseb z nedavno anamnezo zgage 4 tedne zdravljenih z 20 mg esomeprazola. Simptome, povezane z refluksom kisline (kot sta zgaga in kisla regurgitacija), so ocenjevali retrospektivno v 24 urah. V obeh študijah je bil 20 mg esomeprazola bistveno boljši od placeba za primarni cilj popolne razrešitve zgage, opredeljen kot odsotnost zgage v 7. dni pred zadnjim obiskom (33,9% -41,6% v primerjavi s placebom 11,9% -13,7%, (dnevnik bolnika, bil je statistično pomemben tako v prvem tednu (10, 0% -15,2% v primerjavi s placebom 0,9% -2,4%, p = 0,014, str
Druge sekundarne končne točke so podpirale primarno končno točko, vključno z lajšanjem zgage v 1. in 2. tednu, odstotkom 24-urnih dni brez zgage v 1. in 2. tednu, povprečno resnostjo zgage v 1. in 2. tednu ter časom za dosego prve rešitve zgage v 24 urah in ponoči ter trajno razrešitev zgage v primerjavi s placebom. Približno 78% bolnikov, ki so prejemali 20 mg esomeprazola, je poročalo o razrešitvi zgage v prvem tednu zdravljenja v primerjavi s 52-58% pri placebu. Čas za dosego trajne razrešitve zgage, opredeljen kot prvih 7 zaporednih dni brez zabeležene zgage, je bil v skupini z 20 mg esomeprazola bistveno krajši (39,7% -48,7% na dan 14 v primerjavi s placebom 11,0% -20,2%). Mediana časa do prve razrešitve zgage je bila 1 dan, statistično značilna v primerjavi s placebom v eni študiji (p = 0,048) in blizu pomembnosti v drugi (p = 0,069). Približno 80% noči je bilo prostih. menstruacije in 90% noči so bile v 2. tednu vsake študije brez zgage v primerjavi s 72,4-78,3% v skupini, ki je prejemala placebo. Ocene raziskovalcev o odpravljanju zgage so bile skladne z ocenami preiskovancev in so pokazale statistično pomembne razlike med esomeprazolom (34,7% -41,8%) in placebom (8,0% -11,4%). Raziskovalci so tudi ugotovili, da je bil esomeprazol pri ocenjevanju 2. tedna bistveno učinkovitejši od placeba pri odpravljanju kisle regurgitacije (58,5% -63,6% v primerjavi s placebom 28,3% -37,4%).
Po splošni oceni zdravljenja (OTE) bolnikov v 2. tednu zdravljenja je 78,0-80,7 % bolnikov, ki so jemali 20 mg esomeprazola, poročalo o izboljšanju svojega stanja v primerjavi s 72,4-78,3 % v skupini, ki je prejemala placebo. Večina teh je menila, kako pomembna je ta sprememba iz pomembnega v izjemno pomembnega pri opravljanju njihovih vsakodnevnih dejavnosti (79–86% v 2. tednu).
05.2 Farmakokinetične lastnosti
Absorpcija
Esomeprazol je občutljiv na kislo okolje in se daje peroralno v obliki gastrorezistentnih zrnc. In vivo pretvorba v R-izomer ni pomembna. Esomeprazol se hitro absorbira, največje koncentracije v plazmi se pojavijo približno 1-2 uri po odmerjanju. Skupna biološka uporabnost je 64% po enkratnem odmerku 40 mg in se po večkratnem dnevnem odmerjanju poveča na 89% .Za 20 mg odmerek esomeprazola so ustrezne vrednosti 50% oziroma 68% .L Vnos hrane zavira in zmanjša absorpcijo esomeprazola, čeprav to nima pomembnega vpliva na učinek esomeprazola na kislost želodca.
Distribucija
Navidezni volumen porazdelitve v stanju dinamičnega ravnovesja pri zdravih osebah je približno 0,22 l / kg telesne mase. 97% esomeprazola se veže na beljakovine v plazmi.
Biotransformacija
Esomeprazol se v celoti presnavlja s sistemom citokroma P450 (CYP). Večina presnove esomeprazola je odvisna od polimorfno izraženega CYP2C19, ki je odgovoren za tvorbo hidroksi- in desmetilnih presnovkov esomeprazola. Druga specifična izoforma, CYP3A4, odgovorna za nastanek esomeprazol sulfonata, glavnega presnovka v plazmi.
Odprava
Spodnji parametri odražajo predvsem farmakokinetiko pri posameznikih s funkcionalnim encimom CYP2C19, ki obsežno presnavljajo.
Celotni plazemski očistek je po enkratnem odmerku približno 17 L / h in po večkratnem dajanju približno 9 L / h. Razpolovni čas izločanja iz plazme je približno 1,3 ure po večkratnem dnevnem odmerjanju.Esomeprazol se med odmerki popolnoma izloči iz plazme, pri dajanju enkrat na dan se ne kopiči. Glavni presnovki esomeprazola nimajo vpliva na izločanje želodčne kisline. Skoraj 80% peroralnega odmerka esomeprazola se izloči v obliki presnovkov v urinu, preostanek pa v blatu. Manj kot 1% osnovnega zdravila se nahaja v urinu.
Linearnost / Nelinearnost
Farmakokinetiko esomeprazola so proučevali v odmerkih do 40 mg dvakrat na dan.Površina pod krivuljo plazemske koncentracije in časa se s ponavljajočim dajanjem poveča, kar je odvisno od odmerka in vodi do več kot sorazmernega povečanja AUC po večkratnem dajanju. Ta odvisnost od odmerka in časovna odvisnost sta posledica zmanjšanja presnove prvega prehoda in sistemskega očistka, verjetno zaradi zaviranja encima CYP2C19, ki ga povzroča esomeprazol in / ali njegov sulfonatni presnovek.
Posebna populacija bolnikov
Počasni metabolizatorji
Približno 2,9 ± 1,5% populacije ima nezadostno delovanje encima CYP2C19 in jih imenujejo slabi metabolizatorji.Pri teh posameznikih bo presnovo esomeprazola verjetno kataliziral predvsem CYP3A4. Po večkratnem dnevnem odmerjanju 40 mg esomeprazola je bila povprečna površina pod krivuljo plazemska koncentracija-čas približno 100% večja pri slabih presnavljalcih kot pri osebah s funkcionalnim encimom CYP2C19 (ekstenzivni presnavljalci). Povprečna najvišja plazemska koncentracija je bila približno 60% višja.
Ta opažanja nimajo vpliva na odmerjanje esomeprazola.
Seks
Po enkratnem odmerku 40 mg esomeprazola je povprečna površina pod krivuljo plazemske koncentracije / časa približno 30% večja pri ženskah kot pri moških. Po večkratnem dnevnem odmerjanju niso opazili nobene razlike med spoloma.
Okvara jeter
Presnova esomeprazola pri bolnikih z blago do zmerno okvaro jeter je lahko oslabljena. Hitrost presnove se pri bolnikih s hudo okvaro jeter zmanjša, kar povzroči podvojitev površine pod krivuljo plazemske koncentracije-čas esomeprazola. Zato pri bolnikih s hudo disfunkcijo ne smemo preseči največjega odmerka 20 mg. Pri dajanju enkrat na dan se esomeprazol in njegovi glavni presnovki ne kopičijo.
Ledvična okvara
Študije pri bolnikih z okvarjenim delovanjem ledvic niso bile izvedene. Ker so ledvice odgovorne za izločanje presnovkov esomeprazola, ne pa tudi za izločanje matične spojine, pri bolnikih z okvarjenim delovanjem ledvic ni pričakovati vpliva na presnovo esomeprazola.
Starejši bolniki (stari ≥ 65 let)
Presnova esomeprazola se pri starejših bolnikih (starih od 71 do 80 let) bistveno ne spremeni.
05.3 Predklinični podatki o varnosti
Neklinični podatki na podlagi običajnih študij farmakološke varnosti, toksičnosti pri ponavljajočih se odmerkih, genotoksičnosti in toksičnosti za razmnoževanje in razvoj ne kažejo posebnega tveganja za ljudi.
Neželeni učinki, ki jih v kliničnih študijah niso opazili, so pa bili ugotovljeni pri živalih, izpostavljenih stopnjam, podobnim tistim pri klinični izpostavljenosti in z možnim kliničnim pomenom, so naslednje:
Študije rakotvornosti pri podganah, zdravljenih z racemsko mešanico, so pokazale "hiperplazijo želodčnih ECL celic in karcinoidov. Ti želodčni učinki, opaženi pri podganah, so posledica" visoke, izrazite hipergastrinemije, ki je posledica zmanjšane proizvodnje želodčne kisline in so jo pri podganah opazili po dolgem času. -začasno zdravljenje z zaviralci izločanja želodčne kisline.
06.0 FARMACEVTSKE INFORMACIJE
06.1 Pomožne snovi
Glicerol monostearat 40-55,
hiproloza,
hipromeloza,
železov oksid (rdeče-rjav) (E 172),
železov oksid (rumen) (E 172)
magnezijev stearat,
kopolimerizirana disperzija etil akrilata metakrilne kisline (1: 1) pri 30%,
mikrokristalna celuloza,
sintetični parafin,
makrogol 6000,
polisorbat 80,
krospovidon (tip A),
natrijev stearil fumarat,
sladkorne kroglice (saharoza),
smukec,
titanov dioksid (E 171),
trietil citrat.
06.2 Nezdružljivost
Ni pomembno.
06.3 Obdobje veljavnosti
3 leta
06.4 Posebna navodila za shranjevanje
Shranjujte pri temperaturi do 30 ° C.
Shranjujte v originalnem pretisnem omotu za zaščito pred vlago.
06.5 Vrsta ovojnine in vsebina pakiranja
Aluminijasti pretisni omot. Pakiranja po 7 in 14 tablet.
Na trgu ni vseh navedenih pakiranj.
06.6 Navodila za uporabo in rokovanje
Brez posebnih navodil.
07.0 IMETNIK DOVOLJENJA ZA PROMET
Pfizer Consumer Healthcare Ltd
Ramsgate Road
Sendvič
Kent
CT13 9NJ Združeno kraljestvo
08.0 ŠTEVILKA DOVOLJENJA ZA PROMET
EU/1/13/860/001 - AIC 042922017
EU/1/13/860/002 - AIC 042922029
09.0 DATUM PRVEGA DOVOLJENJA ALI PODALJŠANJA DOVOLJENJA
Datum prve odobritve: 26. avgust 2013
10.0 DATUM REVIZIJE BESEDILA
23. januar 2014